题目内容
8. 某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:
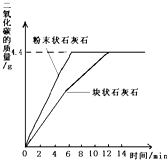
某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:①称取25.0g石灰石样品,平均分成两份,并分别加工成块状和粉末状;②将两份样品分别投入两个锥形瓶中,各加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如图所示.请回答:
(1)由图中曲线分析得出,影响该化学反应速率的因素是:反应物间的接触面积;
(2)每份样品充分反应后.生成二氧化碳的质量为4.4g;
(3)若每份样品中加入l00.0g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数.(要求写出计算过程,不考虑水、氯化氢的逸出.结果精确到0.1%)
分析 (1)反应物接触面积越大,反应越完全,可以据此解答;
(2)根据图象中数据判断出生成二氧化碳的质量;
(3)根据图象中数据二氧化碳的质量计算出碳酸钙的质量和生成的氯化钙的质量,再计算出反应后溶液质量,再用溶质质量除以溶液质量即可.
解答 解:(1)由图中曲线分析,块状和粉末状的碳酸钙在与盐酸反应时,与盐酸的接触面积不同,粉末状的碳酸钙与盐酸接触面积大,反应快;于是得出影响该化学反应速率的因素是:反应物的接触面积;
(2)由图中曲线分析得出,每份样品充分反应后,生成二氧化碳的质量为4.4g;
(3)由图象可知生成二氧化碳质量为4.4g时就不再增加了,说明最多生成4.4g;设每份样品中碳酸钙的质量为x,生成氯化钙的质量为y则:
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
$\frac{100}{x}=\frac{111}{y}=\frac{44}{4.4g}$
解得:x=10g,y=11.1g;
反应后溶液质量为:10g+100g-4.4g=105.6g,
反应后所得溶液中溶质的质量分数为:$\frac{11.1g}{105.6g}$×100%=10.5%;
答案:
(1)反应物间的接触面积;
(2)4.4 g;
(3)反应后所得溶液中溶质的质量分数为10.5%
点评 解答这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,然后根据所给的问题情景结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
15.掌握化学用语是学好化学的关键,下列化学用语与含义不相符的是( )
| A. | 2 个氢原子:2H | |
| B. | 2 个碳酸根离子:2CO32- | |
| C. | 氯化铝:AlCl | |
| D. | 氧化镁中镁元素化合价为+2 价:$\stackrel{+2}{MgO}$ |
16.装运化学药品氢氧化钠的车辆应贴的图标是( )
| A. |  | B. |  | C. |  | D. |  |
13.化学就在我们身边,化学与生活息息相关.
(1)如表为某食品包装袋的部分说明:
请回答下列问题:
①在饼干的配料中,富含蛋白质的是鸡蛋
②碳酸氢钠的俗称小苏打;在医疗上,它是治疗胃酸过多症的一种药剂.
③考虑到营养均衡,把榨好的蔬菜汁放在面粉中和面,做成口味独特、营养丰富的蔬菜馒头,这种馒头提供的主要营养素是糖类和维生素.
(2)饮用硬度过大的水不利于人体健康,日常生活中常用肥皂水来区分硬水和软水,可用煮沸的方法降低水的硬度.
(3)交警通过酒精检测仪显示的颜色变化,可快速检测出司机是否酒后驾车,其反应原理为2CrO3(红色)+3C2H5OH+3H2SO4═Cr2(SO4)3(绿色)+3CH3CHO+6X,X的化学式为H2O.
(1)如表为某食品包装袋的部分说明:
| 商品名称 | ××饼干 |
| 配料 | 小麦粉、白砂糖、精炼植物油、鸡蛋、食盐、食品添加剂(碳酸氢铵、碳酸氢钠、柠檬酸等) |
| 规格 | 180g |
| 保持期 | 10个月 |
①在饼干的配料中,富含蛋白质的是鸡蛋
②碳酸氢钠的俗称小苏打;在医疗上,它是治疗胃酸过多症的一种药剂.
③考虑到营养均衡,把榨好的蔬菜汁放在面粉中和面,做成口味独特、营养丰富的蔬菜馒头,这种馒头提供的主要营养素是糖类和维生素.
(2)饮用硬度过大的水不利于人体健康,日常生活中常用肥皂水来区分硬水和软水,可用煮沸的方法降低水的硬度.
(3)交警通过酒精检测仪显示的颜色变化,可快速检测出司机是否酒后驾车,其反应原理为2CrO3(红色)+3C2H5OH+3H2SO4═Cr2(SO4)3(绿色)+3CH3CHO+6X,X的化学式为H2O.
3.下列物质的化学式、俗名和分类正确的是( )
| A. | NaHCO3 小苏打 酸 | B. | CaO 熟石灰 氧化物 | ||
| C. | Cu2(OH)2CO3 铜绿 盐 | D. | NaOH 纯碱 碱 |
13.下列叙述正确的是( )
| A. | 氢氧化钠固体易潮解,有腐蚀性,称量时不能直接放在天平的托盘上 | |
| B. | 氧气可以支持燃烧,具有可燃性 | |
| C. | 经常用钢丝球洗刷铝锅,能使之光亮、耐用 | |
| D. | 钢铁闸门浸入水下的部分比靠近水面的部分更容易生锈 |
20.“对比实验”是化学学习中行之有效的思维方法,以下实验没有体现“对比”的是( )
| A. | 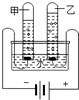 探究水的组成 | B. | 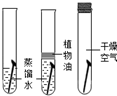 探究铁钉锈蚀的条件 | ||
| C. | 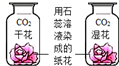 探究CO2的性质 | D. | 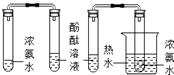 探究分子运动速率与温度关系 |
17.根据所学知识填空:
(1)化学中常用下列词语描述物质的性质:A.可燃性B.吸水性C.溶解性D.还原性.请用序号填空:
①浓硫酸常用作干燥剂是因为它具有B.②氢气作为燃料是因为它具有A.
③焦炭用来冶炼金属D.④能否用排水法收集气体是根据气体的C.
(2)如图是超市里一种盐汽水的营养成分表.
营养成分表
①该汽水中能量主要由碳水化合物提供.该汽水中含人体每天所需的六大营养素有3种.
②“钠115毫克”是指元素(填“单质”或“元素”)的质量.
③小虎同学欲探究该盐汽水的酸碱性,取少量汽水于试管中,滴加紫色石蕊试液,石蕊试液变红色,则该汽水显酸性,经查阅资料该汽水中溶有大量的CO2,要提高100mL水中CO2的溶解量,可加压、降温(写两种方法即可).
(1)化学中常用下列词语描述物质的性质:A.可燃性B.吸水性C.溶解性D.还原性.请用序号填空:
①浓硫酸常用作干燥剂是因为它具有B.②氢气作为燃料是因为它具有A.
③焦炭用来冶炼金属D.④能否用排水法收集气体是根据气体的C.
(2)如图是超市里一种盐汽水的营养成分表.
营养成分表
| 项目 | 每100毫升 | 单位 | 营养素参考值% |
| 能量 | 43 | 千焦 | 1% |
| 蛋白质 | 0 | 克 | 0% |
| 脂肪 | 0 | 克 | 0% |
| 碳水化合物 | 25 | 克 | 1% |
| 钠 | 115 | 毫克 | 6% |
②“钠115毫克”是指元素(填“单质”或“元素”)的质量.
③小虎同学欲探究该盐汽水的酸碱性,取少量汽水于试管中,滴加紫色石蕊试液,石蕊试液变红色,则该汽水显酸性,经查阅资料该汽水中溶有大量的CO2,要提高100mL水中CO2的溶解量,可加压、降温(写两种方法即可).
18.草木灰是农家肥料,主要含钾盐.请回答相关问题.
【分离提纯】
Ⅰ.在烧杯里放一定量的草木灰,加入水,同时用玻璃棒搅拌.
Ⅱ.把烧杯中的草木灰连同浸出液一起过滤.
Ⅲ.把滤液倒入蒸发皿里,加热,用玻璃棒搅拌.当蒸发到大量固体析出_时,停止加热.
【定性分析】取分离提纯所得的晶体进行实验.
【实验反思】
(1)实验一中发生反应的化学方程式有K2CO3+2HCl=2KCl+H2O+CO2↑,CO2+Ca(OH)2=CaCO3↓+H2O.
(2)为证明实验二中的溶液呈碱性是由CO32-引起的,再向红色溶液中加入过量的氯化钙溶液,当看到红色逐渐消失,且溶液中产生白色沉淀时即可证明.
(3)草木灰不能与下列化肥中的C(填“序号”)混合使用.
A.CO(NH2)2 B.KNO3 C.NH4Cl D.磷矿粉
【定量分析】测定草木灰中碳酸钾的含量(假设草木灰中的杂质不含碳酸根,不与酸反应)
测定原理:利用图一中的A装置将草木灰中的碳酸钾转化成二氧化碳,通过测定二氧化碳的质量或体积,计算出草木灰中的碳酸钾的质量.
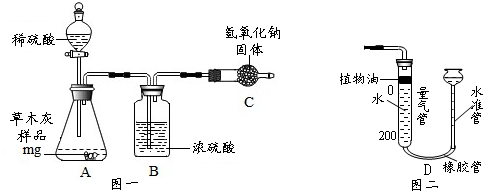
(4)实验前,向图一A的分液漏斗中加入水,用弹簧夹夹住A、B间的橡胶管….这样做的目的是检查装置的气密性;装置B的作用是吸水.
(5)图一装置中欲测定生成的二氧化碳的质量,需测定的数据是C在反应前后的质量.
(6)图二中的D装置可用于测定生成的二氧化碳的体积,测定时不需要(“需要”、“不需要”)等A、B装置中的空气排尽时再连接.
(7)用图一测出的碳酸钾的质量分数偏小,可能的原因是产生的二氧化碳未完全被C吸收.
【分离提纯】
Ⅰ.在烧杯里放一定量的草木灰,加入水,同时用玻璃棒搅拌.
Ⅱ.把烧杯中的草木灰连同浸出液一起过滤.
Ⅲ.把滤液倒入蒸发皿里,加热,用玻璃棒搅拌.当蒸发到大量固体析出_时,停止加热.
【定性分析】取分离提纯所得的晶体进行实验.
| 实验序号 | 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 取样,加入足量的稀盐酸,将生成的气体通入澄清的石灰水 | 石灰水变浑浊 | 该晶体中含有碳酸根离子 |
| 实验二 | 取样,溶于水滴入酚酞 | 溶液变红色 | 溶液呈碱性 |
(1)实验一中发生反应的化学方程式有K2CO3+2HCl=2KCl+H2O+CO2↑,CO2+Ca(OH)2=CaCO3↓+H2O.
(2)为证明实验二中的溶液呈碱性是由CO32-引起的,再向红色溶液中加入过量的氯化钙溶液,当看到红色逐渐消失,且溶液中产生白色沉淀时即可证明.
(3)草木灰不能与下列化肥中的C(填“序号”)混合使用.
A.CO(NH2)2 B.KNO3 C.NH4Cl D.磷矿粉
【定量分析】测定草木灰中碳酸钾的含量(假设草木灰中的杂质不含碳酸根,不与酸反应)
测定原理:利用图一中的A装置将草木灰中的碳酸钾转化成二氧化碳,通过测定二氧化碳的质量或体积,计算出草木灰中的碳酸钾的质量.

(4)实验前,向图一A的分液漏斗中加入水,用弹簧夹夹住A、B间的橡胶管….这样做的目的是检查装置的气密性;装置B的作用是吸水.
(5)图一装置中欲测定生成的二氧化碳的质量,需测定的数据是C在反应前后的质量.
(6)图二中的D装置可用于测定生成的二氧化碳的体积,测定时不需要(“需要”、“不需要”)等A、B装置中的空气排尽时再连接.
(7)用图一测出的碳酸钾的质量分数偏小,可能的原因是产生的二氧化碳未完全被C吸收.