题目内容
20.“对比实验”是化学学习中行之有效的思维方法,以下实验没有体现“对比”的是( )| A. | 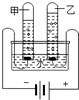 探究水的组成 | B. | 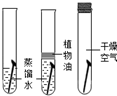 探究铁钉锈蚀的条件 | ||
| C. | 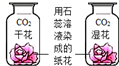 探究CO2的性质 | D. | 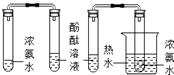 探究分子运动速率与温度关系 |
分析 A.根据电解水的实验现象以及结论来分析;
B.根据探究铁的锈蚀条件来分析;
C.根据探究二氧化碳的性质来分析;
D.根据探究分子运动速率与温度的关系来分析.
解答 解:A.电解水时,甲试管中产生的气体较多,是氢气;乙试管产生的气体较少,是氧气,由此可得出的结论是水是由氢元素与氧元素组成的,没有涉及到对比实验;
B.由第一只和第三只试管对比可知,第一只中的铁与水和氧气充分接触,容易生锈;第三只中的铁只与氧气接触,不容易生锈;通过第一只和第三只对比的现象说明铁生锈必需有水参加;同理,第一只与第二只对比可知,铁的生锈与氧气有关;涉及到了对比实验;
C.此实验中,通过设计湿的纸花和干得纸花变色对比试验,表明了二氧化碳与水能反应的性质,涉及到了对比实验;
D.装置中酚酞溶液变红,说明了分子的一条基本性质是:分子总在不断的运动;设计两组对比实验的目的是:证明温度升高,分子运动速率加快,涉及到了对比实验.
故选A.
点评 对比的方法科学的研究方法,只有明确试验的目的和原理,对实验现象进行综合分析,才能得出正确的结论.

练习册系列答案
相关题目
8.分类法在科学研究中具有广泛的应用.下列说法正确的是( )
| A. | 铝、银均属于金属单质,它们都能与稀硫酸反应 | |
| B. | 金刚石和石墨都是由碳元素组成的单质,它们的原子排列方式相同 | |
| C. | 硫酸铵、氯化铵均属于铵盐,它们都不能跟碱性肥料混合使用 | |
| D. | 一氧化碳、三氧化硫均属于非金属氧化物,它们都能与氢氧化钠溶液反应 |
15.如图是A、B、C三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )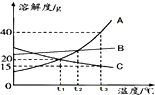

| A. | 温度高于t2℃时,A溶液的溶质质量分数大于B溶液的溶质质量分数 | |
| B. | 要从混有少量B的A溶液中提纯A晶体,操作步骤有蒸发浓缩、降温结晶、过滤等 | |
| C. | t1℃时,将15gA与50g水混合,可以得到65gA溶液 | |
| D. | t3℃时,将饱和的A、B溶液降温至t2℃,析出晶体量A大于B |
12.由氢氧化镁和氧化镁组成的混合物,测得其中含镁元素的质量分数为48%.取该混合物40克,将其投入到适量的稀硫酸中恰好完全反应,所得溶液中溶质的质量为( )
| A. | 24克 | B. | 72克 | C. | 96克 | D. | 48克 |
10.实验室常用的下列仪器中,所用的材料属于复合材料的( )
| A. |  用玻璃棒制作的集气瓶 | B. |  用不锈钢制作的坩埚钳 | ||
| C. |  用塑料制作的药匙 | D. |  用铁丝和石棉的石棉网 |
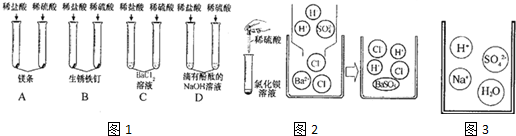
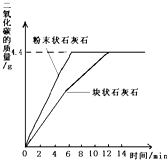 某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:
某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验: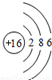 ;(5)最清洁的燃料H2;
;(5)最清洁的燃料H2;