题目内容
13. 请你和小明一起进行食盐水制取二氧化碳的探究
请你和小明一起进行食盐水制取二氧化碳的探究(1)选择药品.小明对三组药品进行了研究,实验记录如下:
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
(2)选择装置.通过对制取氧气装置的分析,他选择用过氧化氢制取氧气的发生装置.你认为他选择的依据是固体和液体反应,不需要加热.
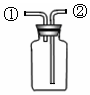
(3)若用如图装置收集CO2,气体应从②进入(填接口序号).
(4)气体检验.将生成的气体通入石蕊溶液中,溶液变红,因此他确定该气体是二氧化碳.他的检验方法是否正确?请说明理由.不正确;其他气体也可能使石蕊溶液变红(或应该用澄清的石灰水检验二氧化碳).
分析 (1)根据化学反应的原理以及化学方程式的写法来分析;
(2)反应物的状态与反应的条件确定了气体的制取装置的选择;
(3)根据二氧化碳的密度比空气大来分析;
(4)根据二氧化碳性质进行验满与气体的检验方案的评价.
解答 解:(1)石灰石的主要成分是碳酸钙,碳酸钙与稀盐酸反应生成氯化钙、水、二氧化碳,故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;
;
(2)由于选择第①组药品反应制取二氧化碳,该组药品为固体和液体在常温下进行反应,与过氧化氢制取氧气反应条件类似,所以选择了相同的发生装置;故填:固体和液体反应,不需要加热;
(3)二氧化碳的密度比空气大,所以用图示装置收集二氧化碳时,二氧化碳从长管进入;故填:②;
(4)检验气体为二氧化碳应把气体通入澄清石灰水,而通入石蕊试液变红不能说明气体为二氧化碳,因为能使石蕊变红的不只有二氧化碳;
故答案为:不正确;其他气体也可能使石蕊溶液变红(或应该用澄清的石灰水检验二氧化碳).
点评 熟练记忆:二氧化碳的实验室制法:固+液,不需加热;反应原理:CaCO3+2HCl═CaCl2+CO2↑+H2O,发生装置和收集装置用到的仪器,以及其检验和验满的方法和操作.学会用探究的方法研究实验问题.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
5.某化合物完全燃烧,消耗2.9g氧气,生成8.8g二氧化碳和5.4g水,该化合物中( )
| A. | 只含有碳和氢两种元素 | B. | 含有碳、氢、氧三种元素 | ||
| C. | 只含有碳氧两种元素 | D. | 无法确定 |
5.对Mg和Mg2+认识不正确的是( )
| A. | Mg和Mg2+是同一种元素 | B. | Mg和Mg2+化合价不同 | ||
| C. | Mg比Mg2+多两个质子 | D. | Mg比Mg2+多两个电子 |
2.某同学在实验室配制溶质质量分数为10%的氢氧化钠溶液,结果所得溶液中溶质氢氧化钠的质量分数为10.8%,请你帮助分析一下最有可能的原因是( )
| A. | 氢氧化钠固体保存不当,已潮解变质 | |
| B. | 用托盘天平称量氢氧化钠固体时,药品与砝码位置放反了 | |
| C. | 用托盘天平称量氢氧化钠时,没有放在玻璃皿中称量 | |
| D. | 用量筒量取水时,俯视水面刻度 |
3.下列现象中,用分子特性解释不合理的选项是( )
| 选项 | 现 象 | 分子特性 |
| A | 充满气的车胎不易压缩 | 分子有一定的质量 |
| B | 10mL酒精与10mL水混合后总体积小于20mL | 分子间有间隔 |
| C | 桌子上的水滴一会儿没有了 | 分子在不断运动 |
| D | 水通直流电产生氢气和氧气 | 分子可以再分 |
| A. | A | B. | B | C. | C | D. | D |
 汽车、电动车一般使用铅酸蓄电池.某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸.请回答下列有关问题:
汽车、电动车一般使用铅酸蓄电池.某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸.请回答下列有关问题:
 如图是3种不同物质的溶解度曲线图,根据图象回答以下问题:
如图是3种不同物质的溶解度曲线图,根据图象回答以下问题: