题目内容
2.被称为“绿色氧化剂”的过氧化氢(H2O2),俗称双氧水,是一种无色的液体,常用做氧化剂、消毒杀菌剂和漂白剂等.在较低温度和少量催化剂(如MnO2)条件下,他能迅速分解,生成氧气和水.请回答下列问题:(1)过氧化氢分解反应的文字表述达是(并写出各物质的化学式):过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;H2O2、MnO2、H2O、O2
(2)若在实验室用过氧化氢代替高锰酸钾制取氧气,能否使用高锰酸钾制取氧气装置,主要理由是用过氧化氢制取氧气不需要加热,用高锰酸钾制取氧气时需要加热.
(3)选择制气装置的依据是反应物状态和反应条件;选择收集气体装置的依据是气体的密度和溶解性.
分析 (1)根据过氧化氢在二氧化锰的催化作用下分解生成水和氧气写出文字表达式即可;根据化学式的书写方法写出各物质的化学式即可;
(2)根据实验室用过氧化氢制取氧气和用高锰酸钾制取氧气的原理进行分析;
(3)发生装置的选择依据反应物状态和反应条件,选择收集装置依据气体的密度和溶解性.
解答 解:(1)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.过氧化氢、二氧化锰、水、氧气的化学式分别为:H2O2、MnO2、H2O、O2;
(2)实验室用过氧化氢制取氧气不需要加热,用高锰酸钾制取氧气时需要加热;
(3)实验室制取气体的装置包括发生和收集装置两部分,发生装置的选择依据反应物状态和反应条件,选择收集装置依据气体的密度和溶解性;
故答案为:(1)过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;H2O2、MnO2、H2O、O2;(2)用过氧化氢制取氧气不需要加热,用高锰酸钾制取氧气时需要加热;(3)反应物状态和反应条件;气体的密度和溶解性.
点评 选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、密度、能否和空气中的物质发生化学反应等因素.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
13.洁净光亮的镁条在二氧化碳中可以燃烧,其化学方程式为:2Mg+CO2 $\frac{\underline{\;点燃\;}}{\;}$ C+2MgO,该反应中具有还原性的是( )
| A. | Mg | B. | CO2 | C. | C | D. | MgO |
10.某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量,实验测得相关数据如图所示:

(1)剩余的混合物中二氧化锰的质量为1g,反应生成氧气的质量为1.6g.
(2)计算参加反应的过氧化氢的质量.

(1)剩余的混合物中二氧化锰的质量为1g,反应生成氧气的质量为1.6g.
(2)计算参加反应的过氧化氢的质量.
11.某兴趣小组同学对实验室制备氧气的若干问题进行如下实验探究.
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲同学设计以下对比实验:
Ⅰ.将2.45g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.通常采用的方法有:
①测相同时间内产生O2的体积
②测收集相同体积O2所需的时间;
Ⅰ中反应的文字表达式是氯酸钾 $→_{加热}^{二氧化锰}$氯化钾+氧气;
Ⅱ中x的值应为2.45.
(2)乙同学用KClO3和MnO2的混合物制取O2,完全反应后的固体残渣,经以下四步实验操作,回收得到了较纯净的MnO2(残渣中只有MnO2难于水).
他的正确操作先后顺序是bcda(填写选项符号).
a.烘干 b.溶解 c.过滤 d.洗涤
步骤 c需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、.
(3)丙同学对课本“分解过氧化氢制氧气的反应中二氧化锰的催化作用”以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣.
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
【实验结论】
(1)A中产生的气体是氧气.
(2)实验II、III证明:氧化铁的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢溶液分解的催化剂.
(3)写出氧化铁催化过氧化氢溶液分解的文字表达式过氧化氢$\stackrel{氧化铁}{→}$水+氧气.
【实验评价】
(1)实验设计IV的目的是进行对比.
(2)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰的催化效果比氧化铁好.
【实验拓展】
(1)查阅资料得知:氧化铜、硫酸铜、马铃薯等也可以做过氧化氢溶液分解的催化剂.下列有关催化剂的说法中正确的是B(填序号).
A.MnO2只能作过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其他反应的反应物或生成物
(2)实验创新是中学生最为重要的科学素养.如图是某学校的师生对“MnO2催化H2O2溶液分解实验装置的创新设计”,实验过程如下:
①将一支球形干燥管水平放置,用滴管吸取3mL(密度为1g/mL)质量分数为5%的H2O2加入干燥管的球泡内,再用药匙取0.2g MnO2粉末,加在干燥管的进气管的管壁上.
②点燃橡胶塞上棒香后,塞紧干燥管并将其竖立,观察到带火星的棒香立即复燃.
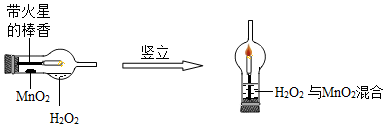
对该创新实验的评价,你认为不合理的是BC(填序号).
A.实验中所用的仪器、材料及药品均易得到
B.实验使用的药品用量太大
C.反应速度太慢,耽误时间
D.实验现象明显,整个装置好似点燃的灯塔,趣味性强.
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲同学设计以下对比实验:
Ⅰ.将2.45g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.通常采用的方法有:
①测相同时间内产生O2的体积
②测收集相同体积O2所需的时间;
Ⅰ中反应的文字表达式是氯酸钾 $→_{加热}^{二氧化锰}$氯化钾+氧气;
Ⅱ中x的值应为2.45.
(2)乙同学用KClO3和MnO2的混合物制取O2,完全反应后的固体残渣,经以下四步实验操作,回收得到了较纯净的MnO2(残渣中只有MnO2难于水).
他的正确操作先后顺序是bcda(填写选项符号).
a.烘干 b.溶解 c.过滤 d.洗涤
步骤 c需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、.
(3)丙同学对课本“分解过氧化氢制氧气的反应中二氧化锰的催化作用”以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣.
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 | 实验现象 |
| I.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象. | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象. | 试管中均产生气泡,带火星木条均复燃 |
| III.将实验 II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag. | / |
| IV.分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象. | / |
(1)A中产生的气体是氧气.
(2)实验II、III证明:氧化铁的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢溶液分解的催化剂.
(3)写出氧化铁催化过氧化氢溶液分解的文字表达式过氧化氢$\stackrel{氧化铁}{→}$水+氧气.
【实验评价】
(1)实验设计IV的目的是进行对比.
(2)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰的催化效果比氧化铁好.
【实验拓展】
(1)查阅资料得知:氧化铜、硫酸铜、马铃薯等也可以做过氧化氢溶液分解的催化剂.下列有关催化剂的说法中正确的是B(填序号).
A.MnO2只能作过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其他反应的反应物或生成物
(2)实验创新是中学生最为重要的科学素养.如图是某学校的师生对“MnO2催化H2O2溶液分解实验装置的创新设计”,实验过程如下:
①将一支球形干燥管水平放置,用滴管吸取3mL(密度为1g/mL)质量分数为5%的H2O2加入干燥管的球泡内,再用药匙取0.2g MnO2粉末,加在干燥管的进气管的管壁上.
②点燃橡胶塞上棒香后,塞紧干燥管并将其竖立,观察到带火星的棒香立即复燃.

对该创新实验的评价,你认为不合理的是BC(填序号).
A.实验中所用的仪器、材料及药品均易得到
B.实验使用的药品用量太大
C.反应速度太慢,耽误时间
D.实验现象明显,整个装置好似点燃的灯塔,趣味性强.
12.2008年5月12日汶川大地震牵动全周人民的心,灾区饮水安全成为人们关注的重要问题.请你运用以下资料及所学的化学知识,为灾区人民提供饮水安全常识.
【资料在线】我国生活饮用水的标准
(1)除去水中难溶性的固体物质可用过滤操作,该操作用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)检验水样是硬水还是软水,可用的物质是肥皂水,若为硬水,其现象是产生的泡沫很少或不产生泡沫,生活中将硬水变为软水的方法是加热煮沸.
【资料在线】我国生活饮用水的标准
| 感官指标 | 化学指标 | 细菌学指标 |
| 水质无色无味 且澄清透明 | pH 6 5~8.5;总硬度<250mg/L.(以碳酸钙计);铜<l 0mg/L,…等 | 细茵总数<100个/mL等 |
(2)检验水样是硬水还是软水,可用的物质是肥皂水,若为硬水,其现象是产生的泡沫很少或不产生泡沫,生活中将硬水变为软水的方法是加热煮沸.
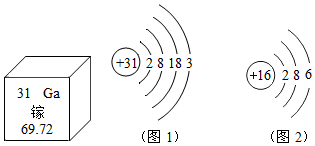 中国最年轻女院士谢毅教授因发现二维超薄半导体在提高光电、热电转换效率方面的工作,获得17届“世界杰出女科学家成就奖”.根据如图中有关镓、硫两种元素信息问答:
中国最年轻女院士谢毅教授因发现二维超薄半导体在提高光电、热电转换效率方面的工作,获得17届“世界杰出女科学家成就奖”.根据如图中有关镓、硫两种元素信息问答:
