题目内容
8.根据碳和碳的氧化物的性质,回答下列问题.(1)重要的签字须用碳素墨水笔,这是因为碳单质常温下化学性质稳定;
(2)冶金工业可利用一氧化碳的还原性来炼铁;
(3)R是最简单的有机物,其燃烧的化学方程式为R+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.则R的化学式为CH4.
分析 (1)据碳的化学性质分析解答;
(2)据一氧化碳的化学性质分析解答;
(3)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物R的化学式.
解答 解:(1)重要的签字须用碳素墨水笔,这是因为碳单质常温下化学性质稳定,不易与其他物质发生化学反应;
(2)一氧化碳具有还原性,所以冶金工业可利用一氧化碳的还原性来炼铁和其他金属;
(3)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式R+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.反应前氧原子个数为4,反应后的生成物中碳、氢、氧原子个数分别为1、4、4,根据反应前后原子种类、数目不变,则每个R分子由1个碳原子、4个氢原子构成,则物质R的化学式为CH4;
故答案为:(1)化学性质稳定; (2)还原; (3)CH4.
点评 本题难度不大,掌握碳的化学性质、一氧化碳的化学性质、利用化学反应前后原子守恒来确定物质的化学式是正确解答此类题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.下列关于水的叙述中正确的是( )
| A. | 通过电解水的实验,说明水是由两个氢原子和一个氧原子构成 | |
| B. | 过滤是降低天然水硬度的简单方法 | |
| C. | 清澈、透明的矿泉水是纯净物 | |
| D. | 吸附、沉淀、过滤和蒸馏等方法都可以净化水 |
19.下列实验现象描述正确的是( )
| A. | 电解水时,正、负电极上产生气体的体积比为2:1 | |
| B. | 木炭在空气中完全燃烧后生成黑色固体 | |
| C. | 铁在氧气中燃烧生成物为熔融状 | |
| D. | 打开一片浓盐酸,瓶口会出现白色烟雾 |
3.下列说法中,错误的是( )
| A. | H2、CO、C具有可燃性,都可以作燃料 | |
| B. | 生石灰、氢氧化钠溶液都能吸收水分,都能作干燥剂 | |
| C. | 浓盐酸、浓硫酸都应密封存放,否则浓度都会变小 | |
| D. | NH4NO3、NH4Cl分别与Ca(OH)2混合研磨都有NH3放出 |
13.以下常州市各文化遗产的生产工艺,主要涉及化学变化的是( )
| A. | 木梳制作 | B. | 黄酒酿造 | C. | 乱针绣 | D. | 竹刻工艺 |
20.取4份等质量的KClO3,向其中3份中分别加入少量等质量的KMnO4、MnO2和Mn,分别在某温度下加热至质量不再改变,测定收集到的氧气质量.然后将剩余固体溶于足量水中,添加过物质的组别中均有相同组成的不溶物.测定结果如下:
已知本题中各反应前后所涉及的含钾元素的化合物均可溶于水.下列说法一定正确的是( )
| 组别 | ① | ② | ③ | ④ |
| 加入物质 | 无 | KMnO4 | MnO2 | Mn |
| 收集到的氧气质量/g | 0 | m1 | m2 | m3 |
| 不溶物的质量/g | 0 | w1 | w2 | w3 |
| A. | 不加入其他物质时,KClO3不能发生分解反应 | |
| B. | KMnO4是KClO3分解制氧气效果最好的催化剂 | |
| C. | 产生氧气的质量关系为m1>m2=m3 | |
| D. | 残留不溶物的质量关系为w1<w2<w3 |
17.生活中的下列变化,有一种与其它在本质上不同的是( )
| A. | 食物腐烂 | B. | 火柴燃烧 | C. | 酒精挥发 | D. | 铁器生锈 |
18.为探究氢氧化钙溶液和稀盐酸反应后所得溶液中溶质的成分,同学们通过测定反应后溶液的PH,得到了如图1所示的PH曲线,请回答下列问题.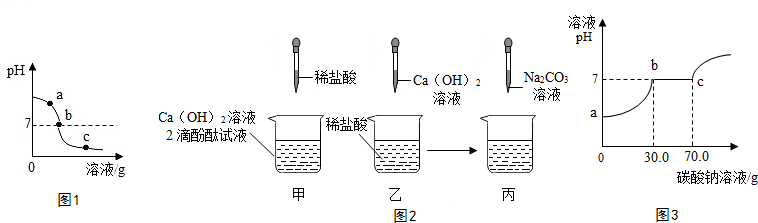
(1)由图1可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,取a、b、c三处反应后的溶液于三个烧杯中,但是忘了做标记,同学们通过设计方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液.
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3═CaCO3↓+2NaCl.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了如表方案:
(4)如图2,同学们做甲、乙、两个中和反应实验的探究.
①甲实验恰好中和,则该溶液中的溶质是CaCl2(化学式).
②取乙反应后的溶液60.0g,滴加质量分数26.5%的Na2CO3溶液,如图2丙,溶液pH的变化如图3,请计算该溶液中CaCl2的溶质质量分数18.5%(写出计算过程,精确到0.1%).

(1)由图1可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,取a、b、c三处反应后的溶液于三个烧杯中,但是忘了做标记,同学们通过设计方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液.
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3═CaCO3↓+2NaCl.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了如表方案:
| 实验步骤 | 实验现象 | 实验结论 |
| 另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液. | 只产生白色沉淀 | 该样品为b处溶液. |
| 先产生气泡,后产生白色沉淀 | 该样品为c处溶液,并推知溶液中的阳离子有Ca2+、H+. |
①甲实验恰好中和,则该溶液中的溶质是CaCl2(化学式).
②取乙反应后的溶液60.0g,滴加质量分数26.5%的Na2CO3溶液,如图2丙,溶液pH的变化如图3,请计算该溶液中CaCl2的溶质质量分数18.5%(写出计算过程,精确到0.1%).
