题目内容
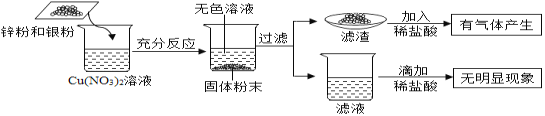
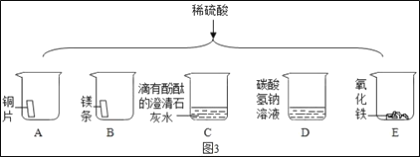
【题目】某白色固体是CuSO4、CaCO3、Ba(NO3)2、Na2SO4、NaOH中的一种或几种.为确定其组成,同学们进行了如下实验.
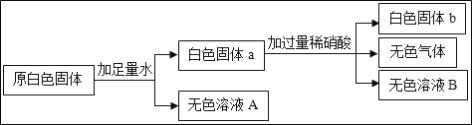
(1)原固体中一定没有___;
(2)实验过程中产生气体的化学方程式为___;
(3)无色溶液B中的溶质是___;
(4)原固体中可能存在的物质是___,要确定其是否存在,还需进行的实验是___.
【答案】CuSO4 CaCO3+2HNO3═Ca(NO3)2+H2O+CO2↑ Ca(NO3)2、HNO3 NaOH 取少量无色溶液A,滴加无色酚酞,变红色则有氢氧化钠
【解析】
(1)硫酸铜溶液为蓝色,所以原白色固体加足量水溶解,得到白色固体和无色溶液,说明一定没有硫酸铜,故填:CuSO4。
(2)硫酸钡沉淀不溶于水、稀硝酸,而碳酸钙沉淀能和硝酸反应生成硝酸钙、水和二氧化碳气体,故反应的化学方程式写为:CaCO3+2HNO3═Ca(NO3)2+H2O+CO2↑。
(3)硫酸钡沉淀不溶于水、稀硝酸,而碳酸钙沉淀能和硝酸反应生成硝酸钙、水和二氧化碳气体,所以加入过量稀硝酸后,无色溶液B中的溶质是硝酸钙和硝酸,故填:Ca(NO3)2、HNO3。
(4)硫酸铜溶液为蓝色,所以原白色固体加足量水溶解,得到白色固体和无色溶液,说明一定没有硫酸铜,硫酸钡沉淀不溶于水稀硝酸,而碳酸钙沉淀能和硝酸反应生成二氧化碳气体,所以加入过量稀硝酸后,还有白色固体,说明固体为硫酸钡,硫酸钡是由硝酸钡和硫酸钠溶液反应生成的,有无色气体生成说明一定含有碳酸钙沉淀,同时还含有硫酸钠和硝酸钡,所以不能确定是否含有氢氧化钠,故填:NaOH;
氢氧化钠溶于水显碱性,能使酚酞试液变红,所以要确定原固体中可能存在的物质,需要进行的实验是取少量无色溶液A,滴加无色酚酞,变红色则有氢氧化钠,故填取少量无色溶液A,滴加无色酚酞,变红色则有氢氧化钠。

【题目】现有一包白色粉末,可能由NH4Cl、Na2CO3、NaHCO3中的一种或几种组成。小莹为了探究其成分,进行了如下实验:
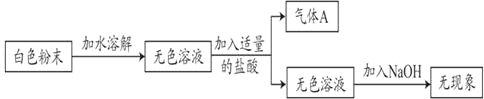
(1)由上述实验可知气体A是_____。
(2)根据上述的实验现象,原白色粉末一定没有_____。
(3)(发现问题)Na2CO3、NaHCO3与盐酸反应,均能产生气体,无法确定固体的成分。
(查阅资料)
①NaHCO3与可溶性的钙盐、钡盐混合没有沉淀产生。
②NaHCO3与足量的Ca(OH)2反应有白色沉淀产生。
(提出猜想)
猜想1:白色粉末只有_____;
猜想2:白色粉末只有Na2CO3;
猜想3:白色粉末是_____。
(实验探究)
小勇为了验证其猜想,取少量的白色粉末放入烧杯中,加水全部溶解后,加入足量的Ca(OH)2溶液,现象是_____,他就认为猜想二正确。小杰认为小勇的结论不正确,理由是_____,
于是他做了进一步的探究:
实验操作 | 现象 | 实验结论 |
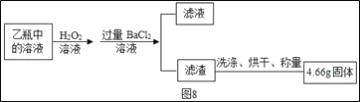
取白色粉末于烧杯中,加水溶解,再加入BaCl2溶液充分搅拌,静置 | 若无_____现象 | 猜想_____成立 |
若_____ | 证明白色固体肯定有_____,可能有_____ | |
取10.6g白色粉末于锥形瓶中,加入足量稀盐酸后把生成的气体通入足量的NaOH溶液中,反应完全后称得NaOH溶液增重4.5g | 确认猜想_____成立 |