题目内容
8.在宏观、微观和符号之间建立联系是化学学科的特点.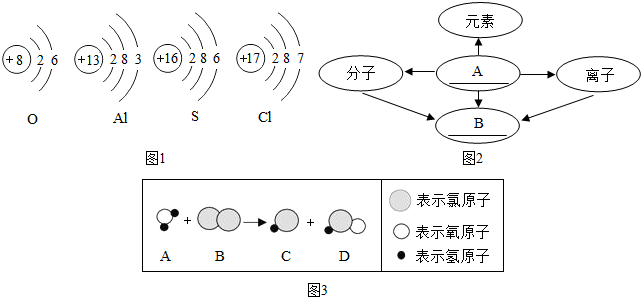
(1)根据下列元素的原子结构示意图1填空.
①氧元素和硫元素化学性质相似的原因是它们的原子最外层电子数相同;
②铝原子在化学反应中易失去(填“得到”或“失去”)电子,由铝元素和氮元素组成化合物的化学式为AlCl3.
(2)某同学对物质组成和结构方面的知识进行了归纳,请你填写空白,完成他的设计,如图2中A是原子,B是物质.
(3)目前有些自来水厂用氯气进行消毒.消毒过程中会发生如下化学反应,其反应的微观过程可用如图3表示:写出图3所示反应的化学方程式Cl2+H2O═HCl+HClO.
分析 (1)根据元素原子的最外层电子数决定了元素的化学性质分析;根据最外层电子数小于4个易失去电子,大于4个易得到电子分析得失电子情况,从而确定元素的化合价,再根据化合价书写化学式即可;
(2)根据分子、原子、离子、元素与物质之间的关系可填写图中的空;
(3)根据质量守恒定律可以正确书写化学方程式.
解答 解:
(1)①元素原子的最外层电子数决定了元素的化学性质,氧元素和硫元素化学性质相似的原因是它们的原子最外层电子数相同,故填:最外层电子数;
②铝元素原子的最外层电子数是3,在化学反应中易失去3个电子带3个单位的正电荷,其化合价为+3价,氯元素原子的最外层电子数是7,在化学反应中易得到1个电子带一个单位的负电荷,其化合价为-1价,因此由铝元素和氯元素组成化合物的化学式为AlCl3;故填:AlCl3;
(2)原子得失电子可转化为离子,原子构成分子,具有相同核电荷数的一类原子称为元素;而分子、原子、离子都可构成物质,故可填:A原子、B物质;
(3)由图中可知,一个氯气分子和一个水分子反应生成一个氯化氢分子和一个次氯酸分子,反应的化学方程式为:Cl2+H2O═HCl+HClO;
答案:
(1)①最外层电子数;②失去;AlCl3;
(2)A:原子;B:物质;
(3)Cl2+H2O═HCl+HClO.
点评 掌握物质分类的知识、原子结构示意图所表示出的信息和意义以及书写化学式时要注意正价在前,负价在后,正负化合价代数和为零是解决此题的关键,难度较大.

练习册系列答案
相关题目
3.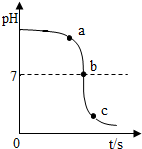 某校化学小组在利用稀硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )
某校化学小组在利用稀硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )
 某校化学小组在利用稀硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )
某校化学小组在利用稀硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )| A. | 图中c点所示溶液呈碱性 | |
| B. | 图中a点所示溶液中,含有的溶质是Na2SO4和H2SO4 | |
| C. | 若将实验中的稀硫酸改为其溶质质量分数相同的稀盐酸,恰好完全反应时消耗稀盐酸质量小于稀硫酸 | |
| D. | 由a点到b点的pH变化过程证明酸和碱发生了中和反应 |
13.为了测定液化气中的丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如表:
(1)丙烷中碳、氢元素质量比为9:2;表中a为5.6g;
(2)4.4g丙烷中所含碳元素质量与13.2g二氧化碳所含碳元素质量相等.
| 物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
(2)4.4g丙烷中所含碳元素质量与13.2g二氧化碳所含碳元素质量相等.
20.同学们对制作糕点常用膨松剂Na2CO3或NaHCO3进行了下列探究.
【查阅资料】
【探究一】NaHCO3和Na2CO3性质差异的探究
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液
酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显蓝色;
酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
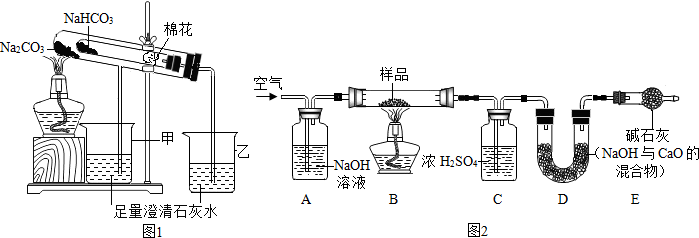
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,
甲烧杯不变,则乙烧杯中发生反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.1.5g B.0.96g C.0.5g
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)
【问题讨论】
(4)实验前先通一段时间的空气的目的是排尽装置内的空气(或二氧化碳);
(5)A的作用是吸收鼓入空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(6)停止加热后,仍继续通入空气一段时间,目的是使反应生成的二氧化碳全部被D吸收.
【含量测定】
(7)测得装置D的质量实验前为120.2g,实验后为122.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(8)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O═2NaHCO3.
【查阅资料】
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液
酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显蓝色;
酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,
甲烧杯不变,则乙烧杯中发生反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.1.5g B.0.96g C.0.5g
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)

【问题讨论】
(4)实验前先通一段时间的空气的目的是排尽装置内的空气(或二氧化碳);
(5)A的作用是吸收鼓入空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(6)停止加热后,仍继续通入空气一段时间,目的是使反应生成的二氧化碳全部被D吸收.
【含量测定】
(7)测得装置D的质量实验前为120.2g,实验后为122.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(8)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O═2NaHCO3.
17.小明同学探究铜锌合金做成的“金戒指”中铜元素的含量,取8g的“金戒指”,在老师的指导下,将“金戒指”经浓硝酸氧化、碱化等步骤处理后,最终得到纯净的氧化铜,称得质量仍然为8g(实验过程中铜元素损失忽略不计).则“金戒指”中铜元素的质量分数是( )
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
18.逻辑推理是化学学习中常用的思维方法,推理正确的是( )
| A. | 碱的水溶液通常呈碱性,所以碱性溶液一定是碱的溶液 | |
| B. | 单质是由同种元素组成的纯净物,所以由同种元素组成的纯净物一定是单质 | |
| C. | 分子是构成物质的微粒,所以物质一定都是由分子构成的 | |
| D. | 有机物都含碳元素,所以碳元素的化合物都是有机物 |