题目内容
3.实验是科学探究的重要方式.请完成下列探究:
(1)如图1:把二氧化碳气体慢慢倒入离低不同的燃着蜡烛的烧杯中,现象是蜡烛都熄灭且下层的蜡烛先熄灭,本实验中放置两支蜡烛的目的是验证二氧化碳的密度比空气大.
(2)分别向集满空气和呼出气体的集气瓶中倒入澄淸石灰水,并充分振荡发现二者的变化有明显的不同,写出有关的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
(3)某同学探究二氧化碳的性质如图2:先在烧钚内壁上贴上干的和湿的紫色石蕊纸条,再将充满二氧化碳的敞口集气瓶轻轻放入烧杯中.一段时间后.现象是湿的紫色石蕊纸条变红色;本实验可以说明的分子运动论的知识是分子在不断运动;烧杯内壁贴的干的石蕊纸条起对照作用,目的是证明二氧化碳不能使紫色石蕊变红;该实验可得出的结论是CO2+H2O=H2CO3(用化学方程式表示).
分析 (1)根据二氧化碳的物理性质、化学性质进行分析解答即可.
(2)根据实验的现象分析结论;
(3)根据分子是不断运动的分析回答;根据实验的过程和现象分析回答烧杯内壁上贴干的紫色石蕊纸条的目的;根据实验的过程和现象分析该实验得出的结论.
解答 解:(1)将一瓶二氧化碳气体慢慢倒入燃着蜡烛的烧杯中,观察到的现象是下层的蜡烛火焰先熄灭,上层的蜡烛火焰后熄灭,这是因为CO2密度比空气大、不能燃烧、不能支持燃烧;故答案为:蜡烛都熄灭且下层的蜡烛先熄灭;验证二氧化碳的密度比空气大;
(2)呼出的气体中二氧化碳的含量高,加入石灰水后,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,所以看到盛有呼出气体的烧杯内澄清的石灰水变浑浊;故填:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)一段时间后,由于分子具有的性质是分子在不断地运动,观察到湿的紫色石蕊纸条变为红色;烧杯内壁上贴干的紫色石蕊纸条不变色,说明了二氧化碳不能使紫色石蕊变红;该实验得出的结论是二氧化碳和水反应生成碳.故填:湿的紫色石蕊纸条变红色;分子在不断运动;对照;二氧化碳不能使紫色石蕊变红;CO2+H2O=H2CO3.
点评 本题的难度不大,考查了二氧化碳的性质以及分子的特征等了解分子是不断运动的,二氧化碳能与水化合生成了碳酸是解答本题的基础知识.

练习册系列答案
相关题目
11.根据下表数,回答问题.
(1)20℃KNO3的溶解度是31.6g;
(2)60℃时,200gKNO3溶液中含质100g.将该溶液降温至20℃,可析出KNO368.4g;
(3)NaCl溶液中含有少量KNO3,提纯NaCl,采用的方法是蒸发结晶.(填“降温结晶”或“蒸发结晶”).
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 25.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(2)60℃时,200gKNO3溶液中含质100g.将该溶液降温至20℃,可析出KNO368.4g;
(3)NaCl溶液中含有少量KNO3,提纯NaCl,采用的方法是蒸发结晶.(填“降温结晶”或“蒸发结晶”).
8.t℃时,在足量的碳酸钠饱和溶液中加人ag无水碳酸钠,可析出mg碳酸钠晶体,则(m-a)的值是( )
| A. | 饱和溶液失去溶剂的质量 | B. | 减少的饱和溶液的质量 | ||
| C. | 析出无水物的质量 | D. | 饱和溶液失去溶质的质量 |
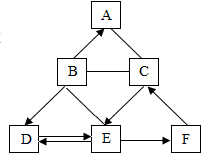 图中A~F为初中化学常见的六种物质,其中A、B、D含相同的阴离子,C、D、E、F含有同一种元素,C、E、F是不同类别的物质.A、C之间的反应可用于检验铵态氮肥,B、E之间的反应是实验室制取二氧化碳的反应原理.框图中“-”表示相连的两种物质间能发生化学反应,“→”表示物质间存在转化关系(部分反应物、生成物及反应条件已略去).回答下列问题:
图中A~F为初中化学常见的六种物质,其中A、B、D含相同的阴离子,C、D、E、F含有同一种元素,C、E、F是不同类别的物质.A、C之间的反应可用于检验铵态氮肥,B、E之间的反应是实验室制取二氧化碳的反应原理.框图中“-”表示相连的两种物质间能发生化学反应,“→”表示物质间存在转化关系(部分反应物、生成物及反应条件已略去).回答下列问题:



