题目内容
19.实验室常用如图1的装置来制取氧气:
(1)写出图1中有标号仪器的名称:a酒精灯、b铁架台;
(2)用高锰酸钾制取氧气时,可选用的发生装置是A(填序号);其反应类型为分解反应.
(3)用E装置收集氧气的依据是气体密度比空气大,检验氧气是否集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则气体已经集满;
(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水.制取并收集NH3,应该从上图中选择的发生装置是A,收集装置是D;(填序号)
(5)在医院里给病人输氧时,在氧气钢瓶和病人吸氧器之间连接一个类似图2所示的装置,在装置中盛放大约半瓶蒸馏水,导气管a(填“a”或“b”)端连接在供氧气的钢瓶上.
分析 (1)从仪器的图和用途去分析;
(2)从加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,反应需要加热分析;
(3)从氧气的密度比空气大,氧气的验满方法去分析.
(4)用氯化铵固体与碱石灰固体共热来制取氨气的发生装置为“固体加热型”进行选择;常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,氨气极易溶于水,进行选择收集装置.
(5)根据氧气的密度的大小关系分析进气口.
解答 解:(1)由仪器的图和用途可知a为酒精灯,b为铁架台;故答案为:酒精灯;铁架台;
(2)用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,所以化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,其反应类型为分解反应;由于反应需要加热,所以发生装置应选A;
(3)由于氧气的密度比空气大,所以可用向上排空气法收集;氧气的验满方法是:带火星的木条,放在集气瓶口,如果复燃,证明已满;
(4)用氯化铵固体与碱石灰固体共热来制取氨气的发生装置为“固体加热型”,因此发生装置选择:A;
常温下氨气密度比空气小,氨气极易溶于水,因此不能用排水法收集,应用向下排空气法收集,故选 D;
(5)在医院里给病人输氧时,在氧气钢瓶和病人吸氧器之间连接一个类似图2所示的装置,在装置中盛放大约半瓶蒸馏水,由于氧气的密度比水小,导气管a端连接在供氧气的钢瓶上.
故答案为:
(1)酒精灯;鉄架台; (2)A;分解;
(3)气体密度比空气大; 将带火星的木条放在集气瓶口,若木条复燃,则气体已经集满.
(4)A; D (5)a.
点评 实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度,主要考查了实验室制取氧气的反应原理,及注意事项,是考试的重点也是中考的重点.

 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案| A. | 汽油挥发 | B. | 滴水成冰 | C. | 矿石粉碎 | D. | 橡胶老化 |
| A. | 碳酸钙粉末 | B. | 酒精 | C. | 泥沙 | D. | 植物油 |
| A. | 能使无色酚酞试液变色 | |
| B. | 能使紫色石蕊试液变红色 | |
| C. | 电离时生成的阳离子全部是氢离子的化合物 | |
| D. | 能与碳酸盐反应生成二氧化碳 |
 化学小组同学设计了下列兴趣实验.
化学小组同学设计了下列兴趣实验.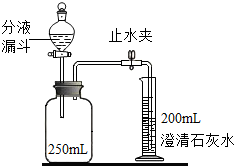
 某同学为研究动物的呼吸作用,用如图所示的方式进行实验.实验过程中发现澄清石灰水变浑浊,红墨水向左(填“左”或“右”)移动,实验结束后将燃着的木条放到瓶中,木条熄灭.说明动物呼吸时吸进氧气气体,呼出二氧化碳气体.
某同学为研究动物的呼吸作用,用如图所示的方式进行实验.实验过程中发现澄清石灰水变浑浊,红墨水向左(填“左”或“右”)移动,实验结束后将燃着的木条放到瓶中,木条熄灭.说明动物呼吸时吸进氧气气体,呼出二氧化碳气体.