题目内容
15.某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液.现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g.请计算:(1)生成氧气的质量;
(2)瓶内过氧化氢溶液中溶质的质量分数;
(3)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液1000g,需加入水的质量.
分析 根据质量守恒定律计算出氧气的质量,然后根据化学方程式结合物质间的质量关系进行分析解答即可.
解答 解:(1)生成氧气的质量为:34g+3g-33.8g=3.2g;
(2)设参与反应的过氧化氢的质量为x.
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$ 2H2O+O2↑
68 32
x 3.2g
$\frac{68}{32}=\frac{x}{3.2g}$
x=6.8g
瓶内过氧化氢溶液中溶质的质量分数为:$\frac{6.8g}{34g}×100%=20%$
(3)设需瓶内溶液的质量为y.
20%×y=1000g×3%
y=150g
需加入水的质量为:1000g-150g=850g
答:(1)生成氧气的质量为3.2g;(2)瓶内过氧化氢溶液中溶质的质量分数为20%;(3)需加入水的质量为850g.
点评 本题考查的是根据化学方程式的计算,解题的关键是根据质量守恒定律计算出氧气的质量.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
3.下列图示的实验操作中错误的是( )
| A. |  气密性的检查 气密性的检查 | B. | 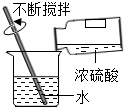 稀释浓硫酸 稀释浓硫酸 | ||
| C. |  铁丝在氧气中燃烧 铁丝在氧气中燃烧 | D. |  测定空气的组成 测定空气的组成 |
4.下列说法中,正确的是( )
| A. | 合金被广泛的使用,是因为合金比组成它们的纯金属具有更多优良性能 | |
| B. | 人体缺少必须微量元素会得病,因为应尽可能多吃含有这些元素的营养补剂 | |
| C. | 打开汽水瓶盖时,汽水会自动喷出来,说明此时气体在水中的溶解度变大了 | |
| D. | 一氧化碳有毒,燃着的煤炉会产生一氧化碳,在煤炉上放一壶水能防止人中毒 |
10.下列物质中,属于溶液的是( )
| A. | 硬水 | B. | 石灰乳 | C. | 冰水 | D. | 液氧 |
7.类推是化学学习中常用的思维方法.下列类推结果正确的是( )
| A. | 金刚石和石墨都是碳的单质,金刚石能作玻璃刀,所以石墨也能作玻璃刀 | |
| B. | 酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| C. | SO2和CO2都能与水反应生成酸,所以SO2和CO2都能与NaOH溶液反应 | |
| D. | NaOH和Cu(OH)2都是碱,所以它们具有完全相同的性质 |
4.下列各组中物质的俗称、化学名称与化学式表示同一种物质的是( )
| A. | 熟石灰 氧化钙 CaO | B. | 纯碱 氢氧化钠 NaOH | ||
| C. | 酒精 乙醇 C2H5OH | D. | 苏打 碳酸氢钠 Na2CO3 |
 早在春秋战国时期,我们就开始生产和使用铁器.请按要求填空:
早在春秋战国时期,我们就开始生产和使用铁器.请按要求填空: