题目内容
3. 早在春秋战国时期,我们就开始生产和使用铁器.请按要求填空:
早在春秋战国时期,我们就开始生产和使用铁器.请按要求填空:(1)工业上用赤铁矿石炼铁原理的化学方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
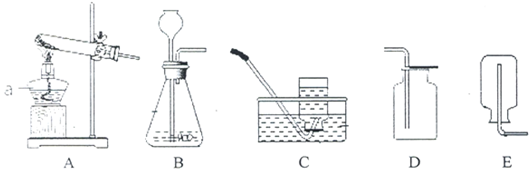
(2)右图实验中,硬质玻璃管中的现象是红色粉末变成黑色;
(3)下列关于金属的叙述,正确的是BCDF.
A.合金中至少有两种金属;
B.合金比组成它们的纯金属硬度更高,熔点更低;
C.合金一定为混合物;
D.保护金属资源可以采用刷漆的方法;
E.工业炼铁,得到的是纯铁
F.工业炼铁所需的原料有铁矿石、焦炭、石灰石和空气.
分析 (1)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳;
(2)一氧化碳具有还原性,与氧化铁反应生成铁和二氧化碳,硬质玻璃管中的红色粉末变成黑色;
(3)根据合金的概念、组成、保护金属资源的措施、炼铁的方法、原料等分析解答.
解答 解:(1)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)一氧化碳具有还原性,与氧化铁反应生成铁和二氧化碳,会观察到硬质玻璃管中的红色粉末变成黑色;故填:红色粉末变成黑色;
(3)A.合金是指在一种金属中加热熔合其他金属或非金属而形成的具有金属特性的物质,所以合金中至少有一种金属,故错误;
B.合金比组成它们的纯金属硬度更高,熔点更低,故正确;
C.合金是由多种物质组成的,一定为混合物,故正确;
D.保护金属资源可以采用刷漆的方法防止金属的锈蚀,故正确;
E.工业炼铁,得到的是铁中含有杂质,属于生铁,故错误;
F.工业炼铁所需的原料有铁矿石、焦炭、石灰石和空气,故正确.
故填:BCDF.
点评 本题难度不大,掌握一氧化碳还原氧化铁的反应原理与注意事项等是正确解答本题的关键.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案
相关题目
11.下列实验能达到实验目的且操作正确的是( )
| A. |  检验溶液酸碱度 | B. |  铁丝在O2中燃烧 | ||
| C. |  测定空气中的O2的含量 | D. |  溶解固体 溶解固体 |
12.化学是你,化学是我,化学深入我们生活,下列说法不正确的是( )
| A. | 皮蛋有碱性,食用时可加点食醋中和 | |
| B. | 用水灭火,目的是降低可燃物的着火点 | |
| C. | 洗涤剂能洗掉油污是因为洗涤剂具有乳化功能 | |
| D. | 硝酸铵能促进植物枝叶生长茂盛,它是一种氮肥 |
9.下列过程中,只发生物理变化的是( )
| A. | 汽油燃烧 | B. | 铜器锈蚀 | C. | 切割大理石 | D. | 葡萄酿酒 |
12.现有氢气、镁、氧化铜、稀硫酸、石灰水、碳酸锌溶液、氯化镁溶液和硝酸钠溶液8种物质,在常温下,它们两两相互发生反应有( )
| A. | 5个 | B. | 6个 | C. | 7个 | D. | 8个 |
13.下列物质的用途与性质对应不正确的是( )
| 物 质 | 用 途 | 性 质 | |
| A | 二氧化碳 | 作气体肥料 | 二氧化碳既不燃烧也不支持燃烧 |
| B | 熟石灰 | 改良酸性土壤 | 熟石灰能与酸发生中和反应 |
| C | 小苏打 | 治疗胃酸过多 | 小苏打能与盐酸反应 |
| D | 氮气 | 焊接金属时做保护气 | 氮气的化学性质不活泼 |
| A. | A | B. | B | C. | C | D. | D |