题目内容
20.某地环保部门对辖区倍盐酸工厂排出的废水进行检测:取50g废水样品,用5%的氢氧化钠溶液中和,当测得pH等于7时,消耗此氢氧化钠溶液质量为8g.求该工厂排放的废水中HCl的质量分数是多少?分析 根据已知条件8g质数分数为5%的氢氧化钠溶液的质量计算出含溶质氢氧化钠的质量,再根据方程式计算出参加反应的氯化氢的质量.
解答 解:
8g 质量分数为5% 的氢氧化钠溶液中氢氧化钠的质量是8g×5%=0.4g
设50g废水中氯化氢的质量为x.
NaOH+HCl═NaCl+H2O
40 36.5
0.4g x
$\frac{40}{36.5}=\frac{0.4g}{x}$
x=0.365g
废水中HCl的质量分数为:$\frac{0.365g}{50g}×100%$=0.73%
答:该工厂排放的废水中HCl的质量分数是0.73%.
点评 解答本题的关键是计算出含纯溶质氢氧化钠的质量,再根据方程式计算出需要参加反应的氯化氢的质量.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
9.下列过程中,只发生物理变化的是( )
| A. | 汽油燃烧 | B. | 铜器锈蚀 | C. | 切割大理石 | D. | 葡萄酿酒 |
5.关于下列四种粒子的结构示意图的说法中正确的是( )
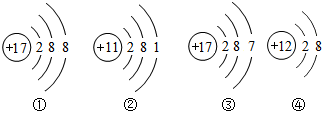

| A. | ①③属于不同种元素 | |
| B. | ②表示的元素在化合物中通常显+1价 | |
| C. | ②③的化学性质相似 | |
| D. | ④属于离子,离子符号为Mg+2 |
12.现有氢气、镁、氧化铜、稀硫酸、石灰水、碳酸锌溶液、氯化镁溶液和硝酸钠溶液8种物质,在常温下,它们两两相互发生反应有( )
| A. | 5个 | B. | 6个 | C. | 7个 | D. | 8个 |
9.实验室有甲、乙两种金属粒和一瓶硝酸银溶液.李明同学将过量的甲、乙两种金属粒分别放入两支盛有少量硝酸银溶液的试管中,发现两支试管中均有金属银析出.李明将试管中的溶液分别过滤,然后又取了一些金属粒甲分别放入过滤好的溶液中,她观察到两支试管中都没有明显变化.下列关于此次实验的说法中正确的是( )
| A. | 金属甲一定是铁 | |
| B. | 金属乙在金属活动性顺序表中一定排在氢前面 | |
| C. | 甲、乙两种金属的活动性顺序是:甲<乙 | |
| D. | 银的金属活动性顺序大于甲、乙两种金属 |
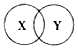 化学概念间有不同的关系,如包含、并列、交叉关系等.下列选项符合如图所示关系的是( )
化学概念间有不同的关系,如包含、并列、交叉关系等.下列选项符合如图所示关系的是( )