题目内容
13.如图所表示的实验方法或操作中正确的是( )| A. |  加锌粒 | B. |  实验室制取CO2 | ||
| C. |  称量固体 | D. |  验证质量守恒定律 |
分析 A、根据取用块状固体药品时的注意事项进行分析;
B、根据实验室制取CO2的方法进行分析;
C、根据使用托盘天平称量固体时的注意事项进行分析;
D、根据验证质量守恒定律的方法进行分析.
解答 解:A、取用块状固体药品时,先将试管横放,用镊子把固体放在试管口,再让试管慢慢地竖起来,故A操作错误;
B、实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,故B操作正确;
C、使用托盘天平称量固体时,氢氧化钠是易潮解的药品,应该放在玻璃器皿中称量,故C操作错误;
D、盐酸与铁粉会生成氢气,而逸出,不利于证明质量守恒定律,应放在密闭容器中,故D操作错误.
故选B.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
4.“舌尖上的安全、味蕾上的健康”,下列做法合理的是( )
| A. | 购买包装食品时关注生产日期和保质期 | |
| B. | 发霉的花生蒸煮后可食用 | |
| C. | 用亚硝酸钠代替食盐烹调食物 | |
| D. | 用福尔马林保鲜海产品 |
8. 如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
(1)依据如表数据,绘制Ca(OH)2和NaOH的溶解度曲线,上图中能表示NaOH溶解度曲线的是A(选填“A”或“B”).
(2)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到乙溶液,此时溶液中溶质的质量分数:甲>乙(选填“>”“<”或“=”).
(3)现有Ca(OH)2和NaOH两种溶质的混合溶液,若要得到较纯净的NaOH溶液,应加入适量Na2CO3溶液.
(4)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH偏小(选填“偏大”“偏小”或“不受影响”).
 如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
(2)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到乙溶液,此时溶液中溶质的质量分数:甲>乙(选填“>”“<”或“=”).
(3)现有Ca(OH)2和NaOH两种溶质的混合溶液,若要得到较纯净的NaOH溶液,应加入适量Na2CO3溶液.
(4)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH偏小(选填“偏大”“偏小”或“不受影响”).
18.下列变化中属于物理变化的是( )
| A. | 葡萄酿成酒 | B. | 湿法冶铜 | C. | 煤的燃烧 | D. | 风力发电 |
5.下列推理正确的是( )
| A. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的物质一定是化合物 | |
| B. | 分子、原子都是不带电的粒子,但是不带电的粒子不一定是分子、原子 | |
| C. | 碱溶液一定能使酚酞试剂变红,能使酚酞试剂变红的一定是碱溶液 | |
| D. | 中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应 |
2. 在一定质量的甲溶液中逐渐加入乙物质至过量,反应过程中溶液的总质量与加入乙的质量的关系与如图曲线相符的是 ( )
在一定质量的甲溶液中逐渐加入乙物质至过量,反应过程中溶液的总质量与加入乙的质量的关系与如图曲线相符的是 ( )
 在一定质量的甲溶液中逐渐加入乙物质至过量,反应过程中溶液的总质量与加入乙的质量的关系与如图曲线相符的是 ( )
在一定质量的甲溶液中逐渐加入乙物质至过量,反应过程中溶液的总质量与加入乙的质量的关系与如图曲线相符的是 ( )| 序号 | 甲 | 乙 |
| A | CuSO4溶液 | 铁粉 |
| B | H2SO4溶液 | 锌粒 |
| C | HCl溶液 | NaOH溶液 |
| D | CaCl2溶液 | Na2CO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
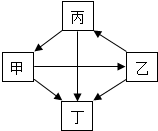 金属元素形成的化合物,依据物质的组成常见为氧化物、碱、盐,甲、乙、丙、丁均是由钙元素形成的四种常见化合物,丙、丁属于盐,另两种物质分别是氧化物和碱,它们之间的转化关系如图(部分反应物和产物已略去,“→”表示物质间存在转化关系).请回答
金属元素形成的化合物,依据物质的组成常见为氧化物、碱、盐,甲、乙、丙、丁均是由钙元素形成的四种常见化合物,丙、丁属于盐,另两种物质分别是氧化物和碱,它们之间的转化关系如图(部分反应物和产物已略去,“→”表示物质间存在转化关系).请回答