题目内容
18.下列排序正确的是( )| A. | 地壳中元素的含量 | B. | 溶液的pH | ||
| C. | 硫元素的化合价 | D. | 溶解时放出的热量 |
分析 A、根据地壳中元素的含量分析解答;
B、根据当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性;据此进行分析判断即可;
C、根据在化合物中正负化合价代数和为零,分别计算选项中硫元素的化合价,进行解答;
D、根据物质溶于水时的温度变化分析解答.
解答 解:
A、地壳中元素的含量为:O、Si、Al、Fe、Ca,故错误;
B、汽水呈酸性,pH小于7,食盐水呈中性,pH等于7,肥皂水呈碱性,pH大于7,溶液的pH由小到大为:汽水<食盐水<肥皂水,故错误;
C、氢显+1价,设H2S中硫元素的化合价为a,根据在化合物中正负化合价代数和为零,则:(+1)×2+a=0,解得a=-2;
S单质中元素的化合价为0,
氧显-2价,氢显+1价,设H2SO4中硫元素的化合价为b,根据在化合物中正负化合价代数和为零,则(+1)×2+b+(-2)×4=0,解得b=+6;
硫元素的化合价由高到低为:H2SO4>S>H2S,故错误;
D、氢氧化钠溶于水放热,温度升高,氯化钠溶于水温度不变,硝酸铵溶于水吸热,温度降低,溶解时放出的热量由多到少为:氢氧化钠>氯化钠>硝酸铵,故正确.
答案:D
点评 本题难度不大,掌握地壳中元素的含量、溶液的酸碱性和溶液pH大小之间的关系、化合物中正负化合价代数和为零是顺利解题的关键.

练习册系列答案
相关题目
8.请你根据如图所示的溶解度曲线判断,下列说法中正确的是( )
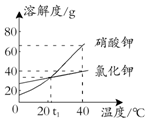

| A. | 氯化钾在20℃时的溶解度比硝酸钾大 | |
| B. | 将40℃的硝酸钾溶液降温至20℃,溶液中一定会有晶体析出 | |
| C. | 将等量的氯化钾和硝酸钾分别放于等量的水中,把温度调为t1℃,此时,二者的溶质质量分数相等 | |
| D. | 当温度高于t1℃时,饱和硝酸钾的溶剂质量分数比饱和氯化钾的大 |
6.下列实验操作中,不正确的是( )
| A. |  加热液体 | B. |  稀释浓硫酸 | C. |  蒸发食盐水 蒸发食盐水 | D. |  熄灭酒精灯 |
13.下列物质的用途与化学性质对应的是( )
| 选项 | A | B | C | D |
| 用 途 |  |  |  |  |
| 干冰用于人工降雨 | 活性炭作口罩滤芯 | 碳棒(含石墨)作电极 | 蜡烛在空气中燃烧 | |
| 性质 | 干冰升华吸热性 | 活性炭吸附性 | 石墨导电性 | 氧气助燃性 |
| A. | A | B. | B | C. | C | D. | D |
3.进行下列对比试验,不需要控制变量的是( )
| A. | 用氯化钙溶液检验某氢氧化钠溶液是否变质 | |
| B. | 用红磷和白磷探究可燃物燃烧的条件 | |
| C. | 用铁钉探究铁生锈的条件 | |
| D. | 用镁、锌与稀硫酸反应,比较镁、锌的金属活动性强弱 |
7.铁的锈蚀对社会生产造成较大损害,但也有有利的一面,如某些食品包装袋内常放入还原性铁粉作“双吸剂”以防止食品腐败.某课外兴趣小组在实验室发现了一包破损的还原性铁粉(含少量杂质,杂质既不溶于水也不溶于酸),他们取六份样品,分别加稀硫酸反应.测得部分数据加下,请根据有关信息回答问题.
(1)m的数值为0.1.
(2)第3次实验,所得到溶液中溶质的化学式为Fe2(SO4)3、FeSO4.
(3)列式计算该样品中单质铁的质量分数(保留至0.1%).
| 实验次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 取样品质量(g) | 31.0 | 31.0 | 31.0 | 31.0 | 31.0 | 31.0 |
| 取稀硫酸质量(g) | 30.0 | 90.0 | 120.0 | 150.0 | 180.0 | 210.0 |
| 产生气体质量(g) | 0 | m | 0.3 | 0.5 | 0.6 | 0.6 |
(2)第3次实验,所得到溶液中溶质的化学式为Fe2(SO4)3、FeSO4.
(3)列式计算该样品中单质铁的质量分数(保留至0.1%).