题目内容
14.某元素R的微粒结构的意图为: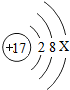
该元素的原子核外有17个电子,X的最大值是8.
分析 根据原子结构示意图的意义及核外电子排布的规律进行分析:小圆圈和圈内的数字表示原子核和核内质子数;弧线表示电子层,弧线上的数字该电子层上的电子数,最外层的电子数不超过8个(第一层为2个).
解答 解:由R的微粒结构的意图可知,该元素的原子核内有17个质子,为氯元素;原子的质子数=电子数,故该元素的原子核外有17个电子;X是最外层上的电子数不超过8个,所以,X的最大值是8.
故答为:17,;8.
点评 本题的难度不大,理解微粒结构示意图的意义、正确书写微粒的符号是解答本题的基础.

练习册系列答案
相关题目
4.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
下列说法中不正确的是 ( )
| 物质 | X | Y | Z | Q |
| 反应前的质量/g | 4 | 10 | 1 | 25 |
| 反应后的质量/g | 待测 | 21 | 10 | 9 |
| A. | X的待测值为零 | B. | 该反应遵守质量守恒定律 | ||
| C. | 反应中Y和Z质量比为11:9 | D. | 该反应属于分解反应 |
9.2015年9月我国天津塘沽码头集装箱着火,解放军官兵赶到现场灭火,直接用水去扑灭火,火没有扑灭反而引起了爆炸,用水扑灭的目的是( )
| A. | 使温度降到着火点以下 | B. | 隔绝氧气 | ||
| C. | 隔绝可燃物 | D. | 隔绝空气 |
19.氮化硅(Si3N4)是一种新型陶瓷材料的主要成分.氮化硅属于( )
| A. | 单质 | B. | 化合物 | C. | 氧化物 | D. | 混合物 |
4.红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图1所示.
同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究】甲同学的方案:
乙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色,并设计如图2实验方案继续验证.

②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.乙同学对滤渣B又进行探究.
同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究】甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放于试管中,滴加足量的稀盐酸. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe,一定不含Fe2O3. |

②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.乙同学对滤渣B又进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| ①取滤渣B于试管中,加入适量稀盐酸 ②将生成的气体通入澄清石灰水 | ①固体减少,有气泡冒出,溶液变为黄色. ②澄清石灰水变浑浊 | 固体中一定含有CaCO3 和Fe2O3 |


