题目内容
3.某同学为测定一瓶失去标签的氢氧化钠溶液的溶质质量分数,取80g该氢氧化钠溶液,逐滴加入10%的稀硫酸至pH等于7,测得反应后溶液的总质量为129g.计算:该氢氧化钠溶液的溶质的质量分数.分析 根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.所以参与反应的稀硫酸的质量=反应后溶液的总质量-氢氧化钠溶液的质量,据此列出比例式,就可计算出氢氧化钠溶液中所含的氢氧化钠的质量分数.
解答 解:稀硫酸中H2SO4的质量为:(129g-80g)×10%=4.9g,
设氢氧化钠溶液中所含的氢氧化钠质量为x
H2SO4+2NaOH═Na2SO4+2H2O
98 80
4.9g x
$\frac{98}{4.9g}$=$\frac{80}{x}$
x=4g
所以氢氧化钠溶液的溶质的质量分数为:$\frac{4g}{80g}$×100%=5%.
故答案为:5%.
点评 本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
13.下列实验现象描述正确的是( )
| A. | 红磷在空气中燃烧产生大量白雾 | |
| B. | 硫在氧气中燃烧发出明亮的蓝紫色火焰 | |
| C. | 电解水实验中,正极产生的气体体积是负极的2倍 | |
| D. | 碳在空气中燃烧生成二氧化碳 |
11.根据如图微粒结构示意图给出的信息,下列说法错误的是( )
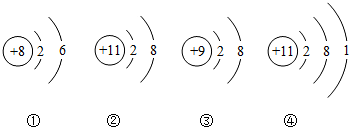
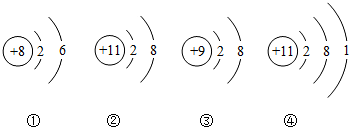
| A. | 粒子③是阴离子 | B. | 粒子②和④属于同种元素 | ||
| C. | 粒子②和③的化学性质相对稳定 | D. | ①元素通常显+2价 |
15.t℃时,将一定量KNO3的不饱和溶液平均分为三份,分别恒温蒸发出水的质量为5g、10g、15g,析出KNO3晶体的质量依次为a g、b g、c g,则a、b、c三者的关系为( )
| A. | c=a+b | B. | c=2b-a | C. | c=a+2 b | D. | c=2 a-b |
12.下列有关四个基本反应类型的说法,正确的是( )
| A. | 化合反应一定只有一种生成物 | |
| B. | 有单质参加的反应一定是置换反应 | |
| C. | 分解反应一定有气体生成 | |
| D. | 生成两种化合物的反应一定是复分解反应 |
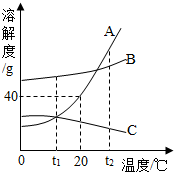 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答: