题目内容
8.观察和实验是学习化学的重要方式,下列实验现象的描述中,正确的是( )| A. | 硫在氧气中燃烧产生微弱的淡蓝色火焰,生成无色无味的气体 | |
| B. | 红磷在空气中燃烧产生大量的白雾 | |
| C. | 打开装有浓盐酸的试剂瓶的瓶塞,在瓶口上方观察到白烟 | |
| D. | 把洁净的铜丝插入硝酸银溶液中,一段时间后溶液由无色逐渐变为蓝色 |
分析 A、据硫在氧气中燃烧的现象分析判断;
B、据红磷在空气中燃烧的现象分析判断;
C、据浓盐酸具有挥发性分析判断;
D、据铜丝和硝酸银反应的现象分析判断.
解答 解:A、硫在氧气中燃烧产生明亮的蓝紫色火焰,生成无色有刺激性气味的气体,故错误;
B、红磷在空气中燃烧产生大量的,而非白雾,故错误;
C、打开装有浓盐酸试剂瓶的瓶塞,瓶口上方有白雾产生,而非白烟,故错误.
D、把洁净的铜丝放入硝酸银溶液中,溶液由无色逐渐变为浅蓝色,铜丝表面有银白色固体析出,故选项正确.
故选:D.
点评 本题难度不大,掌握常见物质燃烧的现象、及浓盐酸具有挥发性、金属的化学性质即可正确解答;在描述物质燃烧的现象时,需要注意烟和雾的区别.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
16.“三效催化转换器”可将汽车尾气中有毒气体处理为无污染的气体,如图为该反应的微观示意图(其中不同符号的球代表不同的原子).下列说法正确的是( )
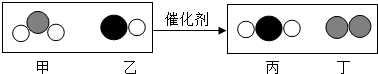

| A. | 乙物质由两个元素组成. | |
| B. | 甲和丁中同种元素化合价不相等 | |
| C. | 该反应中涉及到的最小微粒是分子 | |
| D. | 化学方程式中乙、丁的物质的量之比为1:1 |
3.为验证某混合气体中是否含有一氧化碳、二氧化碳和水蒸气,同学设计了如图实验装置 (装置气密性良好),将混合气体依次通入,实验现象记录如下.(药品均足量且每步反应完全、夹持仪器省略)

①丙中粉末由黑变红,发生的化学反应方程式为CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
②丁装置中发生的化学反应方程式为CO2+H2O=H2CO3;
③根据上述现象,分析混合气体中一定含有水蒸气、一氧化碳,可能含有二氧化碳.写出可能含有二氧化碳的理由甲增重,一定含有水蒸气,氧化钙和水反应生成氢氧化钙,氢氧化钙可与二氧化碳反应;
④在不改变装置的前提下,只需将装置甲中药品换成无水硫酸铜,即可判断二氧化碳是否存在;
⑤经过④中改进后,装置依然存在问题,继续改进的方法是在乙和丙之间加加一个盛有氢氧化钠溶液的洗气瓶.

| 装置 | 现象 |
| 甲 | 增重 |
| 乙 | 无明显现象 |
| 丙 | 粉末由 黑变红 |
| 丁 | 试液由紫变红,气球变大 |
②丁装置中发生的化学反应方程式为CO2+H2O=H2CO3;
③根据上述现象,分析混合气体中一定含有水蒸气、一氧化碳,可能含有二氧化碳.写出可能含有二氧化碳的理由甲增重,一定含有水蒸气,氧化钙和水反应生成氢氧化钙,氢氧化钙可与二氧化碳反应;
④在不改变装置的前提下,只需将装置甲中药品换成无水硫酸铜,即可判断二氧化碳是否存在;
⑤经过④中改进后,装置依然存在问题,继续改进的方法是在乙和丙之间加加一个盛有氢氧化钠溶液的洗气瓶.
13. 如图是电解水的微观模型图,从中获得的信息不正确的是( )
如图是电解水的微观模型图,从中获得的信息不正确的是( )
 如图是电解水的微观模型图,从中获得的信息不正确的是( )
如图是电解水的微观模型图,从中获得的信息不正确的是( )| A. | 在化学反应中,分子可以再分,原子不能再分 | |
| B. | 每个水分子由2个氢原子和1个氧原子构成 | |
| C. | 水分解过程中,原子的种类、分子的种类都不变 | |
| D. | 在化学反应中,元素的种类和质量都不改变 |
20.用X、Y分别表示两种金属,在溶液中能发生反应X+2YNO3=X(NO3)2+2Y,下列说法中不正确的是( )
| A. | 该反应属于置换反应 | |
| B. | 若X是Cu,Y是Ag,则反应后溶液质量减少 | |
| C. | X可能是Fe,Y可能是Cu | |
| D. | X的金属活动性比Y强 |


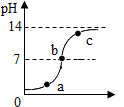 酸碱可以发生中和反应,生成盐和水,如图是硫酸溶液和氢氧化钠溶液反应过程中溶液的pH变化,请写出从图中获取的信息:
酸碱可以发生中和反应,生成盐和水,如图是硫酸溶液和氢氧化钠溶液反应过程中溶液的pH变化,请写出从图中获取的信息: