题目内容
17. 如图是四种粒子的结构示意图.
如图是四种粒子的结构示意图.(1)A、B、C、D四种粒子中,属于同种元素的是AC(填字母序号,下同),化学性质相似的是BD.
(2)B在化学反应中易得到(填“得到”或“失去”)电子变成O2-(填符号).
(3)由A与D两种元素组成的物质的化学式为Na2S,该物质由离子(填“分子”“原子”或“离子”)构成.
分析 (1)根据元素的定义和微粒的最外层电子数的特点进行分析解答.
(2)B微粒的解耦股和最外层电子数的特点分析;
(3)根据A与D两种元素写出化学式判段构成无的微粒.
解答 解:(1)A、B、C、D四种粒子中,A、C的质子数相同,属于同种元素,B、D的最外层电子数相同,化学性质相似;
(2)B的最外层电子数是6,大于4,在化学反应中易得到电子变成氧离子,符号为:O2-.
(3)由微粒的构成可知,A属于钠元素,D为硫元素,两种元素组成的物质为硫化钠,化学式为Na2S,该物质由离子构成.
故答为:(1)AC,BD;(2)得到,O2-;(3)Na2S,离子.
点评 本题难度不大,明确粒子中粒子结构示意图的含义、核内质子数和核外电子数之间的关系是正确解题的关键.

练习册系列答案
相关题目
12.下列与质量守恒定律有关的说法正确的是( )
| A. | 铝丝在氧气中燃烧后质量增加,不符合质量守恒定律 | |
| B. | 100g冰融化后质量仍为100g,符合质量守恒定律 | |
| C. | 某物质在空气中燃烧生成了 H2O和CO2,则该物质中一定含有C、H、O三种元素 | |
| D. | 化学反应前后原子的种类、数目和质量都不变,因此化学反应都遵守质量守恒定律 |
11.下图所示的实验操作,正确的是( )
| A. | 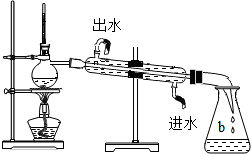 制取蒸馏水 制取蒸馏水 | B. | 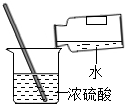 稀释浓硫酸 | ||
| C. | 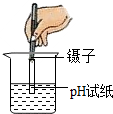 测溶液的pH | D. |  称取氢氧化钠固体 |


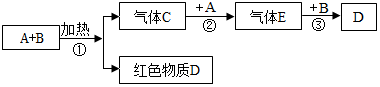

 ”表示氧原子.则物质“
”表示氧原子.则物质“ ”的类型属于下列中的c(填字母序号).
”的类型属于下列中的c(填字母序号). 医生给病人输液时,常用葡萄糖注射液或氯化钠注射液,有时根据病情,也可用葡萄糖复化钠注射液.如图所示的是这种注射液的部分标签.
医生给病人输液时,常用葡萄糖注射液或氯化钠注射液,有时根据病情,也可用葡萄糖复化钠注射液.如图所示的是这种注射液的部分标签.