题目内容
20.将镁、锌、铁、铜四种金属放入相同的稀盐酸中,能观察到有气泡生成的是镁、锌、铁,其剧烈程度由大到小的顺序是镁、锌、铁,不能观察到有气泡生成的是铜,有关化学方程式Mg+2HCl═MgCl2+H2↑、Zn+2HCl═ZnCl2+H2↑、Fe+2HCl═FeCl2+H2↑.由此可知,四种金属的活动性由强到弱的顺序是镁、锌、铁、铜.分析 根据只有排在氢前面的金属才能与酸发生置换反应,生成盐和氢气,且位置越靠前,反应越剧烈;
解答 解:由于金属与酸能否反应以及反应的剧烈程度,可以比较金属活动性强弱,其中镁、锌、铁位于氢前,都能与盐酸反应,而铜位于氢后,不能反应,且镁与盐酸反应最剧烈,产生气泡的速率最快,其次是锌,最慢的是铁,铜与盐酸不反应,可得出的金属活动性强弱顺序为镁>锌>铁>铜.
故答案为:镁、锌、铁;镁、锌、铁;铜;Mg+2HCl═MgCl2+H2↑、Fe+2HCl═FeCl2+H2↑;Zn+2HCl═ZnCl2+H2↑、镁、锌、铁、铜.
点评 本题难度不大,主要考查了金属活动性顺序的应用,熟记金属活动性顺序是解题的关键,能够培养学生对知识的应用能力.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
5.下列关于溶液的叙述正确的是( )
| A. | 任何溶液中只可能含有一种溶质 | |
| B. | 饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 | |
| C. | 溶液一定是均一、稳定、澄清、透明的 | |
| D. | 一杯食盐水,下半部分的比上半部分的咸 |
9.掌握物质的分类是学好化学的基础,指出下列物质中不属于盐的是( )
| A. | HCl | B. | NH4N03 | C. | KClO3 | D. | CuSO4 |
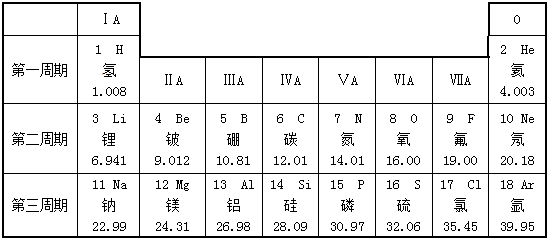
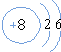 ,该微粒是元素周期表中的氧元素,核电荷数是8,碳元素的核电荷数是6,因此不同元素的本质区别是核电荷数不同.
,该微粒是元素周期表中的氧元素,核电荷数是8,碳元素的核电荷数是6,因此不同元素的本质区别是核电荷数不同.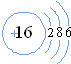 ,在化学反应中易得(填“得”或“失”)电子,是非金属(填“金属”或“非金属”)元素.
,在化学反应中易得(填“得”或“失”)电子,是非金属(填“金属”或“非金属”)元素.