题目内容
久置于空气中因CO2而部分变质的NaOH溶液200g,加入10%的H2SO4溶液147g恰好完全反应,同时产生2.2g气体(全部逸出).试回答下列问题(计算结果保留一位小数):
(1)变质后的新溶质为 (填化学式),其质量为 g,所消耗H2SO4溶质的质量为 g.
(2)变质溶液中NaOH的质量分数是多少?
(1)变质后的新溶质为
(2)变质溶液中NaOH的质量分数是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:二氧化碳能和氢氧化钠反应生成碳酸钠和水,碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳,根据二氧化碳的质量可以计算碳酸钠的质量,同时可以计算消耗的硫酸的质量;
根据硫酸的质量可以计算氢氧化钠的质量,进一步可以计算变质溶液中NaOH的质量分数.
根据硫酸的质量可以计算氢氧化钠的质量,进一步可以计算变质溶液中NaOH的质量分数.
解答:解:(1)变质后的新溶质为碳酸钠,化学式是Na2CO3;
设碳酸钠的质量为x,所消耗H2SO4溶质的质量为y,
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑,
106 98 44
x y 2.2g
=
=
,
x=5.3g,y=4.9g,
故填:Na2CO3;5.3g;4.9g.
(2)设氢氧化钠的质量为z,
和氢氧化钠反应的硫酸的质量为:147g×10%-4.9g=9.8g,
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
z 9.8g
=
,
z=8g,
变质溶液中NaOH的质量分数是:
×100%=4%,
答:变质溶液中NaOH的质量分数是4%.
设碳酸钠的质量为x,所消耗H2SO4溶质的质量为y,
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑,
106 98 44
x y 2.2g
| 106 |
| x |
| 98 |
| y |
| 44 |
| 2.2g |
x=5.3g,y=4.9g,
故填:Na2CO3;5.3g;4.9g.
(2)设氢氧化钠的质量为z,
和氢氧化钠反应的硫酸的质量为:147g×10%-4.9g=9.8g,
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
z 9.8g
| 80 |
| z |
| 98 |
| 9.8g |
z=8g,
变质溶液中NaOH的质量分数是:
| 8g |
| 200g |
答:变质溶液中NaOH的质量分数是4%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2013年1月媒体披露,山西9批含氯处理水的可口可乐被当作合格品出售.使用氯气进行自来水消毒时会发生化学反应,该反应的微观过程可用如图表示:

下列说法不正确的是( )

下列说法不正确的是( )
| A、X表示物质的化学式为HClO |
| B、X物质中氯元素的化合价为+1价 |
| C、反应前后,原子的种类、数目不变 |
| D、该反应中共涉及两种单质和两种化合物 |
 如图为A、B两种物质的溶解度曲线图.请你据图回答下列问题:
如图为A、B两种物质的溶解度曲线图.请你据图回答下列问题: 水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.
水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.
 超市卖的纯碱样品中往往含有少量的氯化钠,某化学兴趣小组的同学通过实验来测定某品牌的纯碱样品中碳酸钠的质量分数.他们取了5g该纯碱样品,在烧杯中配制成60g溶液,再向其中逐滴加入10%的氯化钙溶液,测得加入氯化钙溶液的质量与产生沉淀的质量关系如图所示.请回答下列问题:
超市卖的纯碱样品中往往含有少量的氯化钠,某化学兴趣小组的同学通过实验来测定某品牌的纯碱样品中碳酸钠的质量分数.他们取了5g该纯碱样品,在烧杯中配制成60g溶液,再向其中逐滴加入10%的氯化钙溶液,测得加入氯化钙溶液的质量与产生沉淀的质量关系如图所示.请回答下列问题: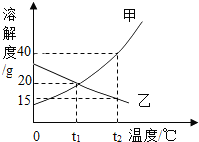 固体甲、乙的溶解度曲线如图所示.
固体甲、乙的溶解度曲线如图所示.