题目内容
为测定氯化镁和氯化钠的混合物中氯化钠的质量分数.一位同学取20g该混合物加入足量的水使其完全溶解,并加入一定量的氢氧化钠溶液,所加氢氧化钠溶液与该样品反应的质量关系如表所示:
求:
(1)第 次恰好完全反应.
(2)混合物中氯化钠的质量分数是多少?
| 实验次数 | ① | ② | ③ |
| 混合物的质量/g | 20 | 20 | 20 |
| 加入氢氧化钠溶液质量/g | 8 | 16 | 24 |
| 产生沉淀质量/g | 2.9 | 5.8 | 5.8 |
(1)第
(2)混合物中氯化钠的质量分数是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:根据表中数据可以判断第几次恰好完全反应;
氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,根据氢氧化镁的质量可以计算氯化镁的质量,进一步可以计算混合物中氯化钠的质量分数.
氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,根据氢氧化镁的质量可以计算氯化镁的质量,进一步可以计算混合物中氯化钠的质量分数.
解答:解:(1)由表中数据可知,向20g混合物中加入16g氢氧化钠溶液时,生成的沉淀是5.8g,继续加入氢氧化钠溶液时,沉淀质量不再增加,因此第②次恰好完全反应.
故填:②.
(2)设氯化镁的质量为x,
MgCl2+2NaOH=Mg(OH)2↓+2NaCl,
95 58
x 5.8g
=
,
x=9.5g,
混合物中氯化钠的质量分数为:
×100%=52.5%,
答:混合物中氯化钠的质量分数为52.5%.
故填:②.
(2)设氯化镁的质量为x,
MgCl2+2NaOH=Mg(OH)2↓+2NaCl,
95 58
x 5.8g
| 95 |
| x |
| 58 |
| 5.8g |
x=9.5g,
混合物中氯化钠的质量分数为:
| 20g-9.5g |
| 20g |
答:混合物中氯化钠的质量分数为52.5%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
下列离子组能在pH=1的无色溶液中大量共存的是( )
| A、NO3- Fe3+ Na+ OH- |
| B、K+ SO42- Na+ NO3- |
| C、Cl- K+ SO42+ Ba2+ |
| D、Ca2+ Cl- CO32- Na+ |
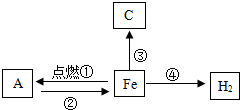 构建知识网络是一种重要的学习方法.如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),C为红色固体单质.请回答下列问题:
构建知识网络是一种重要的学习方法.如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),C为红色固体单质.请回答下列问题: