题目内容
18. 商代的后母戊鼎(原称司母戊鼎)如图,标志着我国在3000年前青铜器铸造已达到一个较高的水平,西汉时期,我国首开“湿法炼铜”之先河,西汉刘安所著的《淮南万毕术》中已有“曾青得铁则化为铜”的记载,试回答下列问题:
商代的后母戊鼎(原称司母戊鼎)如图,标志着我国在3000年前青铜器铸造已达到一个较高的水平,西汉时期,我国首开“湿法炼铜”之先河,西汉刘安所著的《淮南万毕术》中已有“曾青得铁则化为铜”的记载,试回答下列问题:(1)青铜属于合金(选填“单质”或“合金”).
(2)“湿法炼铜”的原理方程式为Fe+CuSO4═Cu+FeSO4;该反应属于置换反应.
(3)铁和铜的金属活动性为:Fe>Cu(选填“>”或“<”)
分析 (1)根据合金是指由一种金属与其它金属或非金属熔合而成的具有金属特性的物质进行分析;
(2)根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(3)根据排在前面的金属可以将排在后面的金属从其盐溶液中置换出来进行分析.
解答 解:(1)青铜属于合金;
(2)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4═Cu+FeSO4,该反应属于置换反应;
(3)排在前面的金属可以将排在后面的金属从其盐溶液中置换出来,所以铁和铜的金属活动性为:Fe>Cu.
故答案为:(1)合金;
(2)Fe+CuSO4═Cu+FeSO4,置换反应;
(3)>.
点评 本题主要考查了化学方程式的书写、判断物质的反应类型及其合金等方面的知识.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
9.如图示意图中,能表示具有稳定结构的原子的是( )
| A. | 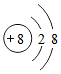 | B. | 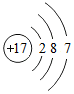 | C. | 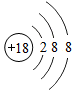 | D. | 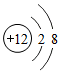 |
6.如表除杂的方法和试剂都正确的是( )
| 选项 | 物质 | 所含的杂质 | 所选试剂和方法 |
| A | HCl | H2SO4 | 加入适量Ba(OH)2溶解、过滤 |
| B | KCl | KClO3 | 加入二氧化锰、加热 |
| C | Cu | CuO | 加入过量的稀盐酸、过滤、洗涤、干燥 |
| D | CaCl2溶液 | Ca(OH)2 | 加入适量的稀硫酸 |
| A. | A | B. | B | C. | C | D. | D |
10.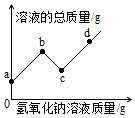 往硫酸和硫酸铜的混合溶液中,逐滴加入氢氧化钠溶液直至过量,根据实验实施绘制如图所示曲线,下列说法正确的是( )
往硫酸和硫酸铜的混合溶液中,逐滴加入氢氧化钠溶液直至过量,根据实验实施绘制如图所示曲线,下列说法正确的是( )
 往硫酸和硫酸铜的混合溶液中,逐滴加入氢氧化钠溶液直至过量,根据实验实施绘制如图所示曲线,下列说法正确的是( )
往硫酸和硫酸铜的混合溶液中,逐滴加入氢氧化钠溶液直至过量,根据实验实施绘制如图所示曲线,下列说法正确的是( )| A. | a至b段有蓝色沉淀生成 | B. | c点溶液中只有1种溶质 | ||
| C. | c至d段,溶液pH不断减小 | D. | d点溶液中只有Na+和SO42- |
7.实验室有一瓶纯碱(Na2CO3)固体中混有少量烧碱(NaOH),现在需要测出这瓶药品中烧碱的含量,便取固体药品12g置于含水100g烧杯中,搅拌至完全溶解,并滴加几滴酚酞试液,溶液呈红色;再滴加稀盐酸,当用去稀盐酸100g时,溶液恰好变成无色. 反应前后质量关系如表:
请回答:
(1)整个反应生成气体4.4g
(2)原固体样品中含纯碱 (Na2CO3)10.6g
(3)计算出使用的稀盐酸的溶质质量分数.
| 反应前 | 反应后 | ||
| 固体样品 | 水 | 稀盐酸 | 剩余液体 |
| 12g | 100g | 100g | 207.6g |
(1)整个反应生成气体4.4g
(2)原固体样品中含纯碱 (Na2CO3)10.6g
(3)计算出使用的稀盐酸的溶质质量分数.