题目内容
8.某氯化钾样品含有杂质氯化钙和氯化镁,设计提纯的流程图如图: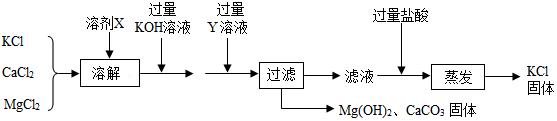
请认真分析流程中各步骤的信息作答:
(1)溶剂X是水(或H2O);
(2)蒸发操作的目的是除去(填物质的化学式)HCl、H2O;
(3)写出加入过量Y溶液反应的化学方程式:K2CO3+CaCl2=CaCO3↓+2KCl.
分析 (1)根据加入X的目的是使样品充分溶解分析试剂;
(2)根据盐酸具有挥发性及蒸发原理分析所除的物质分析;
(3)根据流程图分析,加入氢氧化钾可以除去氯化镁,除去氯化钙而又不增加新的杂质用碳酸钾溶液.
解答 解:(1)加入溶剂X的目的是使样品充分溶解形成溶液,便于实验,因此X是水;故答案为:水(或H2O);
(2)蒸发可以除去溶液中的水分而得到氯化钾固体,而盐酸具有挥发性,可以挥发出氯化氢气体,所以同时还可以除去溶液中的氯化氢;故答案为:HCl、H2O;
(3)根据流程图分析,加入氢氧化钾可以除去氯化镁,除去氯化钙而又不增加新的杂质用碳酸钾溶液;
加入过量碳酸钠溶液反应的化学方程式是K2CO3+CaCl2=CaCO3↓+2KCl;故答案为:K2CO3+CaCl2=CaCO3↓+2KCl.
点评 本题主要考查了物质的提纯实验的相关的操作要领以及物质除杂的原则,要明确流程图中每一步的作用,再结合题意细致分析解答.

练习册系列答案
相关题目
16.下列关于家庭小实验的说法正确的是( )
| A. | 淬火的钢针弯曲制成鱼钩 | |
| B. | 用食盐水除去热水瓶内胆壁上的水垢 | |
| C. | 用10%的烧碱溶液自制“叶脉书签” | |
| D. | 制作简易净水器时,为了达到好的净水效果,活性炭应该放在最上层 |
3.下列物质的用途主要由物理性质决定的是( )
| A. | 稀盐酸用于除锈 | B. | 镁粉用于制作照明弹 | ||
| C. | 铝用于制造铝箔 | D. | 液氧用作火箭助燃剂 |
13.下列关于金属和金属材料的认识错误的是( )
| A. | 赤铁矿的主要成分是Fe2O3 | B. | 地壳中含量最高的金属是铝 | ||
| C. | 回收废旧金属有利于节约金属资源 | D. | 生铁和钢的性能完全相同 |
20.在不用指示剂的情况下,哪一个反应发生时不能观察到明显现象( )
| A. | Na2CO3和稀盐酸 | B. | CuO和稀硫酸 | C. | NaOH和稀硫酸 | D. | Ba(NO3)2和稀硫酸 |
17.2009年春夏之际,世界上多个国家和地区出现了甲型H1N1流感,甲型H1N1流感与普通流感一样“可防可治”.甲型H1N1流感病毒属于( )
| A. | 淀粉 | B. | 蛋白质 | C. | 油脂 | D. | 维生素 |
18.某物质X燃烧的化学方程式为:2X+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O,则X的化学式为( )
| A. | C2H4 | B. | C4H4 | C. | C2H2 | D. | CH |
 商代的后母戊鼎(原称司母戊鼎)如图,标志着我国在3000年前青铜器铸造已达到一个较高的水平,西汉时期,我国首开“湿法炼铜”之先河,西汉刘安所著的《淮南万毕术》中已有“曾青得铁则化为铜”的记载,试回答下列问题:
商代的后母戊鼎(原称司母戊鼎)如图,标志着我国在3000年前青铜器铸造已达到一个较高的水平,西汉时期,我国首开“湿法炼铜”之先河,西汉刘安所著的《淮南万毕术》中已有“曾青得铁则化为铜”的记载,试回答下列问题: