题目内容
6.在经过一段时间只是梳理复习后,小雨兴趣小组的同学们都对曾经学习过的内容有了更加深刻的记忆和深入的思考,他们也意识到实验探究是加强学习效果的好途径.【提出问题】实验室制取二氧化碳气体用什么药品更合适呢?
【实验方案】制取二氧化碳实验内容和现象记录如下,请填写下表格中④的操作空白处
| 序号 | ① | ② | ③ | ④ |
| 操作 |  |  |  |  |
| 现象 | 剧烈反应,产生大量气泡,反应迅速停止 | 产生气泡,持续时间较长 | 产生气泡,速率迅速减慢 | 剧烈反应,产生大量气泡,反应迅速停止,溶液浑浊 |
【拓展思维】(1)实验③的反应速率迅速减慢的原因是生成的硫酸钙微溶于水,罩在了大理石的表面,使反应停止.
(2)将实验①和②进行对比后分析发现,影响化学反应速率快慢的因素是反应物间相互接触面积的大小直接影响到化学反应的速率.
(3)你还知道哪一因素影响化学反应的速率?请举一个相应实例具体说明.
分析 【得出结论】根据反应速度来分析解答;
【拓展思维】(1)根据硫酸钙微溶于水来分析解答;
(2)反应物间相互接触面积的大小直接影响到化学反应的速率;
(3)反应的浓度直接影响化学反应的速率.
解答 解:【得出结论】根据图示可知稀盐酸与大理石反应速度适中便于收集,适合实验室用来制取二氧化碳,反应原理为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
答案:②,速度适中便于收集;CaCO3+2HCl═CaCl2+H2O+CO2↑.
【拓展思维】(1)实验③硫酸与碳酸钙反应生成的硫酸钙微溶于水,反应一段时间后,硫酸钙罩在了大理石的表面,使反应停止;
答案:生成的硫酸钙微溶于水,罩在了大理石的表面,使反应停止.
(2)反应物间相互接触面积的大小直接影响到化学反应的速率;
答案:反应物间相互接触面积的大小直接影响到化学反应的速率;
(3)反应的浓度能影响化学反应的速率,如铁丝在空气中不能燃烧,在氧气中剧烈燃烧,火星四射.答案:反应的浓度能影响化学反应的速率,如铁丝在空气中不能燃烧,在氧气中剧烈燃烧,火星四射.
点评 本题属于二氧化碳的实验室制法的探究,属于基础性的考查,依据浓盐酸的挥发性、二氧化碳的制取原理分析即可.

练习册系列答案
相关题目
20.小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题.她设计并完成了下表所示的探究实验:
(1)请你帮小丽同学填写上表中未填完的空格.
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是对比.
(3)第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验.接下来的实验操作是
倾倒掉反应后的液体,向剩余的固体中重新加人过氧化氢溶液.
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 结论 | 总结 | |||
| 实验一 | 取5mL 5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是产生气体很慢. 反应的文字表达式为: 过氧化氢$\stackrel{二氧化锰}{→}$水+氧气. | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | 二氧化锰加入水中不产生氧气 | |
| 实验三 | 向盛有5mL5%过氧化氢溶液的试管中加入二氧化锰, 伸入带火星的木条 | 有大量气泡产生,带火星的木条迅速复燃 | 二氧化锰能加快过氧化氢的分解 | |
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是对比.
(3)第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验.接下来的实验操作是
倾倒掉反应后的液体,向剩余的固体中重新加人过氧化氢溶液.
17.现在有集气瓶盛装的四瓶无色无味的气体,已知他们分别是:氧气、氮气、二氧化碳和空气,请设计实验将他们鉴别开来(不考虑鉴别开以后,气体是否已经受到污染).
| 实验步骤 | 实验现象 | 实验结论 |
| 1.用带火星的木条分别伸入四个集气瓶中 | 其中一瓶气体能使带火星的木条复燃 | 能使带火星的木条复燃的那一瓶是氧气. |
| 2.往剩余的三个集气瓶中,分别倒入少量澄清石灰水,震荡. | 其中一瓶气体能使澄清的石灰水变浑浊 | 能使澄清石灰水变浑浊的那一瓶是二氧化碳 |
| 3.用燃着的木条伸入剩余的两个集气瓶中. | 其中一瓶气体能使火焰熄灭 | 能使火焰熄灭熄灭的是氮气 |
14.实验测得一些溶液的pH如图所示,其溶液酸性较弱的是( )


| A. | 稀硝酸 | B. | 硼酸 | C. | 氯化钠 | D. | 碳酸钠 |
1.如图所示为某化学反应的微观示意图,下列说法正确的是( )


| A. | 该反应基本类型可能为氧化反应 | |
| B. | 物质甲、乙、丙、丁都是化合物 | |
| C. | 反应前后分子种类和个数都发生了变化 | |
| D. | a g甲与b g乙一定能生成(a+b)g的丙和丁 |
11.下列图象能正确反映实验过程中相应量变化的是( )
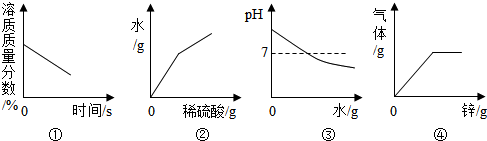

| A. | 图①:将接近饱和的硝酸钾溶液缓慢降温 | |
| B. | 图②:向一定量的氢氧化钡溶液中加过量稀硫酸,生成水的质量与加进稀硫酸的质量关系图 | |
| C. | 图③:向氢氧化钠溶液中加水 | |
| D. | 图④:向一定量的稀硫酸中加入过量的锌 |
18.维生素C又名抗坏血酸,易溶于水,易被氧化,能与碘反应.人体缺乏维生素C可能引发多种疾病.某研究性学习小组对它研究如下:
(1)猜想:维生素C可能具有酸性?
(2)实验方案:
提供试剂:维生素C片、蒸馏水、紫色石蕊试液、无色酚酞试液、稀盐酸、氢氧化钠溶液、氯化钡溶液、pH试纸.
根据以上试剂,请你帮助他们设计出两种实验方案,并写出实验现象:
物质性质的探究
(3)结论:维生素C具有酸性.根据维生素C的性质,判断下列物质中能与维生素C反应的是AC.
A.金属镁 B.食盐 C.氢氧化钠 D.硫酸铜
(4)某同学联想到西红柿等蔬菜、水果中含有丰富的维生素C,放置时间长短是否对维生素C的含量产生影响.他设计了如下实验方案:
Ⅰ把新鲜西红柿和放置一周的西红柿分别捣碎,用纱布将汁液挤入两个烧杯中;
Ⅱ取两支盛有2mL蓝色碘的淀粉溶液的试管,分别滴加上述两种汁液,边加边振荡,直到蓝色刚好消失,记录滴数如下:
请回答下列问题:
①你认为西红柿中维生素C含量高的是新鲜的西红柿.
②你从中得到的启示是尽量吃新鲜的蔬菜水果,西红柿可凉拌食用.
(1)猜想:维生素C可能具有酸性?
(2)实验方案:
提供试剂:维生素C片、蒸馏水、紫色石蕊试液、无色酚酞试液、稀盐酸、氢氧化钠溶液、氯化钡溶液、pH试纸.
根据以上试剂,请你帮助他们设计出两种实验方案,并写出实验现象:
物质性质的探究
| 实 验 内 容 | 实 验 现 象 |
| 方案Ⅰ: | |
| 方案Ⅱ: |
A.金属镁 B.食盐 C.氢氧化钠 D.硫酸铜
(4)某同学联想到西红柿等蔬菜、水果中含有丰富的维生素C,放置时间长短是否对维生素C的含量产生影响.他设计了如下实验方案:
Ⅰ把新鲜西红柿和放置一周的西红柿分别捣碎,用纱布将汁液挤入两个烧杯中;
Ⅱ取两支盛有2mL蓝色碘的淀粉溶液的试管,分别滴加上述两种汁液,边加边振荡,直到蓝色刚好消失,记录滴数如下:
| 汁 液 | 新鲜西红柿的汁液 | 放置一周的西红柿的汁液 |
| 滴 数 | 12 | 20 |
①你认为西红柿中维生素C含量高的是新鲜的西红柿.
②你从中得到的启示是尽量吃新鲜的蔬菜水果,西红柿可凉拌食用.
15.牙膏是生活中常见的物质,其配料成分有摩擦剂、增白剂、发泡剂等,其中摩擦剂的类型有很多,如CaCO3、Al(OH)3、SiO2或这些物质的混合物.我校兴趣小组想研究牙膏摩擦剂的成分.
【提出问题1】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应
【实验方案】
①取少量牙膏于试管中,加入过量稀盐酸,出现气泡,将气体通入澄清石灰水中,石灰水变浑浊,证明摩擦剂中含有碳酸根离子;
②取实验①中的溶液,加入草酸铵【(NH4)2C2O4】溶液,生成白色沉淀--草酸钙,请写出该反应的化学方程式(NH4)2C2O4+CaCl2=CaC2O4↓+2NH4Cl.
【提出问题2】该牙膏中碳酸钙的含量是多少?
【实验步骤】

(1)按图连接好装置后,发现一处明显的错误,改正为C装置中进气管伸入液面以下,出气管稍露出橡皮塞即可;
(2)重新连接好装置,并检查装置的气密性;
(3)在B装置中加入牙膏样品8.00g;
(4)关闭K1,打开K2(填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至B中不再产生气泡,停止滴加盐酸;
(5)关闭K2,打开K1,缓缓通入空气,至C中不再产生沉淀;
(6)将C装置中的固体混合物过滤、洗涤、烘干后称量其质量;
(7)重复实验.
(已知此品牌牙膏中的摩擦剂为碳酸钙,且其他成分不和盐酸反应,装置内试剂均足量.)
【实验数据】重复实验,3次数据记录如下:
【实验分析及数据处理】
(1)上述数据能否由托盘天平测得?(1)不能.
(2)若没有A装置,则测定结果将偏大. (填“偏大”、“偏小”或“不变”)
(3)D装置的作用是吸收空气中的二氧化碳,防止干扰.
(4)据上表数据,计算该牙膏样品中碳酸钙的含量是多少?
写出计算过程.
【实验反思】
(1)重复实验,取平均值的意义在于减小偶然误差(合理即可).
(2)下列各项措施中,能提高测定准确度的是c(填序号)
a.在装置A、B之间增加盛有浓硫酸的洗气瓶
b.在装置B、C之间增加盛有饱和碳酸氢钠的洗气瓶
c.缓缓滴加稀盐酸.
【提出问题1】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应
【实验方案】
①取少量牙膏于试管中,加入过量稀盐酸,出现气泡,将气体通入澄清石灰水中,石灰水变浑浊,证明摩擦剂中含有碳酸根离子;
②取实验①中的溶液,加入草酸铵【(NH4)2C2O4】溶液,生成白色沉淀--草酸钙,请写出该反应的化学方程式(NH4)2C2O4+CaCl2=CaC2O4↓+2NH4Cl.
【提出问题2】该牙膏中碳酸钙的含量是多少?
【实验步骤】

(1)按图连接好装置后,发现一处明显的错误,改正为C装置中进气管伸入液面以下,出气管稍露出橡皮塞即可;
(2)重新连接好装置,并检查装置的气密性;
(3)在B装置中加入牙膏样品8.00g;
(4)关闭K1,打开K2(填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至B中不再产生气泡,停止滴加盐酸;
(5)关闭K2,打开K1,缓缓通入空气,至C中不再产生沉淀;
(6)将C装置中的固体混合物过滤、洗涤、烘干后称量其质量;
(7)重复实验.
(已知此品牌牙膏中的摩擦剂为碳酸钙,且其他成分不和盐酸反应,装置内试剂均足量.)

【实验数据】重复实验,3次数据记录如下:
| 实验次数 | 实验1 | 实验2 | 实验3 |
| C装置中沉淀质量(g) | 3.93 | 3.94 | 3.95 |
(1)上述数据能否由托盘天平测得?(1)不能.
(2)若没有A装置,则测定结果将偏大. (填“偏大”、“偏小”或“不变”)
(3)D装置的作用是吸收空气中的二氧化碳,防止干扰.
(4)据上表数据,计算该牙膏样品中碳酸钙的含量是多少?
写出计算过程.
【实验反思】
(1)重复实验,取平均值的意义在于减小偶然误差(合理即可).
(2)下列各项措施中,能提高测定准确度的是c(填序号)
a.在装置A、B之间增加盛有浓硫酸的洗气瓶
b.在装置B、C之间增加盛有饱和碳酸氢钠的洗气瓶
c.缓缓滴加稀盐酸.
16.下列有关微粒的说法不正确的是( )
| A. | 分子、原子、离子都呈电中性 | |
| B. | 分子、原子和离子都能直接构成物质 | |
| C. | 原子由原子核与核外电子构成 | |
| D. | 原子与离子可以通过得失电子相互转化 |