题目内容
13. 小明同学在化学实验室发现一瓶未知浓度的BaCl2溶液,为测定其浓度他取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液,反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图所示,请计算:
小明同学在化学实验室发现一瓶未知浓度的BaCl2溶液,为测定其浓度他取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液,反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图所示,请计算:(1)若配制26.5%的Na2CO3溶液160g,需要Na2CO3固体21.2g.
(2)根据实验数据,BaCl2溶液的溶质质量分数是多少?(写出计算过程,结果保留到0.1%)
分析 (1)根据溶质质量分数的计算公式,可计算配制26.5%的Na2CO3溶液80g,需要Na2CO3固体的质量;
(2)向BaCl2溶液滴加Na2CO3溶液,二者能发生复分解反应生成沉淀,其方程式为:BaCl2+Na2CO3=BaCO3↓+2NaCl,根据题给数据及图示,利用化学方程式求得BaCl2溶液的溶质质量分数.
解答 解:(1)配制26.5%的Na2CO3溶液80g,需要Na2CO3固体的质量为:80g×26.5%═21.2g
(2)从图中获知,当BaCl2完全转化为沉淀时消耗Na2CO3溶液的质量为40g.
设BaCl2的质量为 x,则
BaCl2+Na2CO3=BaCO3↓+2NaCl
208 106
x 40g×26.5%
$\frac{208}{x}$=$\frac{106}{40g×26.5%}$
解得:x=20.8g
该BaCl2溶液的溶质质量分数为:$\frac{20.8g}{150g}$×100%=13.9%
答:(1)21.2;(2)该BaCl2溶液的溶质质量分数为13.9%
点评 本题是一种综合性的题型,将溶液、化学反应和图象融合在一起,有一定的难度,要求比较高.通常学生在计算时常常会忽视了实际参加反应的是溶液中溶质的质量,而往往会把40g直接代入化学方程式进行计算.这就要求学生足够细心、会分析、且条理分明.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列变化中,属于缓慢氧化的是( )
| A. | 食物腐败 | B. | 硫燃烧 | C. | 铁丝燃烧 | D. | 木炭燃烧 |
18.下列实验操作或对实验现象的描述正确的是( )
| A. | (NH4)2SO4溶液与NaOH溶液混合加热,产生刺激性气味的气体 | |
| B. | 向鸡蛋清溶液中滴加饱和硫酸铵溶液,析出白色固体,是物理变化 | |
| C. | 将浓硫酸倒入量筒,加水稀释,配制100g5%的硫酸溶液 | |
| D. | 蒸发食盐水时,将蒸发皿中水分蒸干后停止加热 |
2.当前食品安全备受人们关注,下列说法会危及人体健康的是( )
| A. | 食用含碘的食盐 | |
| B. | 蒸馒头加适量小苏打 | |
| C. | 用甲醛溶液浸泡海鲜 | |
| D. | 食品袋里充入氮气延长食品的保质期 |


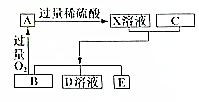 A、B、C、D、E均为初中化学常见的而物质,其中B、C均为金属,B为红色,它们的相对原子质量相差8,D溶液溶质只有一种,E为气体单质,如图是它们之间的相互转化关系,请回答:
A、B、C、D、E均为初中化学常见的而物质,其中B、C均为金属,B为红色,它们的相对原子质量相差8,D溶液溶质只有一种,E为气体单质,如图是它们之间的相互转化关系,请回答: