题目内容
15.图象能直观地反映某些科学规律,下列图象正确的是( )| A. |  电解水得到H2与O2质量关系 | |
| B. |  向稀盐酸中加水,溶液的pH变化 | |
| C. |  向NaOH和Na2CO3混合溶液中逐滴滴加稀盐酸 | |
| D. |  等质量的Mg和Fe与足量相同浓度的稀盐酸反应 |
分析 A、电解水生成氢气和氧气的体积比为2:1,而图象的纵坐标是质量,质量比不等于体积比;
B、根据酸无论如何稀释,pH值会增大,无限的接近7,不会越过7进行分析;
C、向NaOH和Na2CO3混合溶液中逐滴滴加稀盐酸,盐酸先与氢氧化钠反应,再与碳酸钠反应生成二氧化碳;
D、等质量的Mg和Fe与足量相同浓度的稀盐酸反应,镁反应速度快且生成氢气的量多.
解答 解:A、电解水生成氢气和氧气的体积比为2:1,而图象的纵坐标是质量,质量比不等于体积比,错误;
B、酸无论如何稀释,pH值会增大,无限的接近7,不会越过7,错误;
C、向NaOH和Na2CO3混合溶液中逐滴滴加稀盐酸,盐酸先与氢氧化钠反应,再与碳酸钠反应生成二氧化碳,错误;
D、等质量的Mg和Fe与足量相同浓度的稀盐酸反应,镁反应速度快且生成氢气的量多,正确.
故选D
点评 解答本题的关键是要理解图象的物理意义和所代表的反应的反应原理和相关物质的定量反应关系.

练习册系列答案
相关题目
10.在化学世界中,没有生命的阿拉伯数字也变得鲜活起来,它们在不同的位置显示着不同的含义.下列符号中的“2”与3H2中的“2”含义相似的是( )
| A. | Mg2+ | B. | NO2 | C. | $\stackrel{+2}{Ca}$ | D. | 2CO |
20. 探究小组利用如图装置进行四组实验,胶头滴管盛装的是液体,烧瓶中盛装的是气体、固体或液体,当滴管滴几滴液体后,能观察到气球变大的实验组合是( )
探究小组利用如图装置进行四组实验,胶头滴管盛装的是液体,烧瓶中盛装的是气体、固体或液体,当滴管滴几滴液体后,能观察到气球变大的实验组合是( )
 探究小组利用如图装置进行四组实验,胶头滴管盛装的是液体,烧瓶中盛装的是气体、固体或液体,当滴管滴几滴液体后,能观察到气球变大的实验组合是( )
探究小组利用如图装置进行四组实验,胶头滴管盛装的是液体,烧瓶中盛装的是气体、固体或液体,当滴管滴几滴液体后,能观察到气球变大的实验组合是( ) | 组合 | A | B | C | D |
| 滴管中 | Na2CO3 | HCl | NaOH | H2SO4(浓) |
| 烧瓶中 | HCl(液) | Zn(固) | CO2(气) | H2O(液) |
| A. | A | B. | B | C. | C | D. | D |
7.下列实验操作正确的是(??)
| A. | 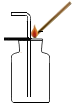 收集二氧化碳并验满 | B. | 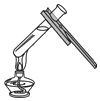 加热液体 | ||
| C. |  取用液体 | D. |  收集氧气 |
5.为了测定某碳酸钠样品(其中杂质为氯化钠)的质量分数,小明同学进行了三次实验,反应的化学方程方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl.实验数据如下表:
根据上表内数据,完成下列有关计算:
(1)碳酸钠样品中碳酸钠的质量是4.24g.
(2)碳酸钠样品中杂质氯化钠的质量分数是15.2%.
(3)加入氯化钙溶液的溶质质量分数是多少?(请根据化学方程式写出完整的计算步骤)
| 编 号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 50 | 50 | 75 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
(1)碳酸钠样品中碳酸钠的质量是4.24g.
(2)碳酸钠样品中杂质氯化钠的质量分数是15.2%.
(3)加入氯化钙溶液的溶质质量分数是多少?(请根据化学方程式写出完整的计算步骤)
 (1)向试管中放入几小粒镁片,把试管底部伸入盛有饱和石灰水(20℃的烧杯中并固定,再向试管中滴入约5ml盐酸,如图所示,结果澄清的饱和石灰水明显变浑浊,这个实验现象产生原因是镁与盐酸反应放出热量使石灰水的温度升高,氢氧化钙的溶解度随温度的升高减小,所以会析出晶体.
(1)向试管中放入几小粒镁片,把试管底部伸入盛有饱和石灰水(20℃的烧杯中并固定,再向试管中滴入约5ml盐酸,如图所示,结果澄清的饱和石灰水明显变浑浊,这个实验现象产生原因是镁与盐酸反应放出热量使石灰水的温度升高,氢氧化钙的溶解度随温度的升高减小,所以会析出晶体. 装满氧气的集气瓶,按右图所示,用带火星的木条分别以甲、乙两种方式迅速插入,发现木条复燃,且在甲中燃烧比在乙更旺.上述实验说明了氧气具有的性质是:(1)氧气的密度比空气的密度大;
装满氧气的集气瓶,按右图所示,用带火星的木条分别以甲、乙两种方式迅速插入,发现木条复燃,且在甲中燃烧比在乙更旺.上述实验说明了氧气具有的性质是:(1)氧气的密度比空气的密度大;