题目内容
14.某中学化学兴趣小组同学在老师的指导下(实验员提供如下器材和若干化学药品),进行气体的制备和性质的探究.
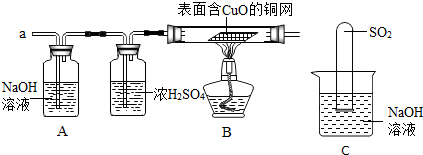
(1)写出图中标号为a的仪器的主要用途收集或储存少量气体.
(2)实验室制取CO2且操作相对简易时,发生装置最好选用AFG(填字母),组装好仪器后,应先检查装置的气密性再添加药品.
(3)实验室常用过氧化氢溶液制氧气,该反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,实验室若需要干燥的氧气,则收集氧气前应先 将氧气通过H装置,H装置中的液体d是浓硫酸,气体通过H时,应从b(填“b”或“c”)端进入.
分析 (1)熟记仪器的名称与用途;
(2)根据实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,组装好仪器,制取气体之前需要检验装置气密性进行分析;
(3)根据过氧化氢在二氧化锰的催化作用下生成水和氧气,浓硫酸有吸水性,洗气应该是长进短出进行分析.
解答 解:(1)仪器a是集气瓶,主要用来收集或储存少量气体;故填:收集或储存少量气体;
(2)实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,所以制取少量二氧化碳可以在试管内进行,塞上单孔塞并固定在铁架台上,实验室制取少量二氧化碳,且操作相对简易时,发生装置最好选用:AFG,组装好仪器,制取气体之前需要检验装置气密性;故填:AFG;检查装置的气密性;
(3)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,浓硫酸有吸水性,洗气应该是长进短出,所以收集氧气前先将气体通过H装置,H装置中的X是浓硫酸,气体通过H时应从b端进入;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,浓硫酸,b.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
相关题目
4.“饮食健康“是人们普遍的生活追求,下列做法正确的是( )
| A. | 用甲醛水溶液浸泡海产品,以防其腐烂 | |
| B. | 在炒熟的菜中放入适量的加碘食盐,使其美味 | |
| C. | 在果汁中加入“塑化剂”,使其口感更好 | |
| D. | 在火腿肠中添加工业用盐亚硝酸钠,使其保持肉质鲜美 |
9.如图表示两种气体发生化学反应,其中相同的球代表同种原子,根据图示信息,下列说法正确的是( )

| A. | 该反应是置换反应 | B. | 该反应生成两种物质 | ||
| C. | 在化学反应前后分子个数一定不变 | D. | 化学反应前后原子种类不变 |
19.化学兴趣小组探究金属的性质时,将一段去除氧化膜的镁条,放入一定量的稀盐酸中,有气泡产生,充分反应后静置,发现试管中有灰白色沉淀.
【提出问题】
灰白色沉淀是什么物质?
【猜想假设】
小华认为灰白色沉淀为碳酸镁(MgCO3),其他同学认为不需要实验就能否定小华的猜想,理由是反应物中没有碳元素,不会生成碳酸镁.
小宇认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体.
小彤认为灰白色沉淀为脱落的镁粉细颗粒.
【实验探究1】
基于以上探究与分析,原有猜想均遭到了否定.
【查阅资料】
HCl+AgNO3═HNO3+AgCl↓,AgCl是一种白色沉淀.
【实验探究2】
他们又另取灰白色沉淀放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了氯化氢气体.再将湿润的蓝色石蕊试纸悬于试管口,试纸变红色.
同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀.据文献介绍,碱式氯化镁存在多种组成结构,化学通式可表示为Mgx(OH)yClz•mH2O(其中2x-y-z=0,0≤m≤6).
【反思拓展】
(1)做镁与稀盐酸反应的实验时,镁条的用量宜少不宜多.
(2)铁片和铜片放入稀硫酸中产生的现象也不相同,据此推测出铁的活性比铜强.还可根据铁和硫酸铜溶液的反应来确定这两种金属的活动性强弱,该反应的化学方程式为Fe+CuSO4=FeSO4+Cu.
【提出问题】
灰白色沉淀是什么物质?
【猜想假设】
小华认为灰白色沉淀为碳酸镁(MgCO3),其他同学认为不需要实验就能否定小华的猜想,理由是反应物中没有碳元素,不会生成碳酸镁.
小宇认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体.
小彤认为灰白色沉淀为脱落的镁粉细颗粒.
【实验探究1】
| 实验操作 | 现象 | 结论 |
| ①取试管中的上层清液,加入适量的氯化镁固体 | 氯化镁固体 溶解(选填“溶解”或“不溶解”) | 小宇猜想错误 |
| ②取适量白色沉淀加入足量稀盐酸中 | 没有(选填“有”或“没有”)气泡冒出 | 小彤猜想错误 |
【查阅资料】
HCl+AgNO3═HNO3+AgCl↓,AgCl是一种白色沉淀.
【实验探究2】
他们又另取灰白色沉淀放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了氯化氢气体.再将湿润的蓝色石蕊试纸悬于试管口,试纸变红色.
同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀.据文献介绍,碱式氯化镁存在多种组成结构,化学通式可表示为Mgx(OH)yClz•mH2O(其中2x-y-z=0,0≤m≤6).
【反思拓展】
(1)做镁与稀盐酸反应的实验时,镁条的用量宜少不宜多.
(2)铁片和铜片放入稀硫酸中产生的现象也不相同,据此推测出铁的活性比铜强.还可根据铁和硫酸铜溶液的反应来确定这两种金属的活动性强弱,该反应的化学方程式为Fe+CuSO4=FeSO4+Cu.
6.化学与生产、生活密切联系,对下列现象或事实解释错误的是( )
| 选项 | 现象或事实 | 解释 |
| A | 洗涤剂能去除衣服上的油污 | 洗涤剂具有乳化作用 |
| B | 用熟石灰改良酸性土壤 | H+和OH-能结合生成H2O |
| C | 水银温度计能指示温度 | 汞原子之间的距离随温度升高而增大 |
| D | 液态二氧化碳可用于图书馆灭火 | 降低图书档案的着火点 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
3.下列有关燃烧、灭火的分析正确的是( )
| A. | 火上浇油:增大可燃物与氧气的接触面 | |
| B. | 钻木取火:提高可燃物的温度达到着火点 | |
| C. | 吹灭烛火:降低着火点 | |
| D. | 电器着火:用水浇灭 |
4.根据下列人体内一些液体的正常的pH范围判断,其中,一定能使石蕊溶液变红的是( )
| A. | 唾液(6.6~7.1) | B. | 胆汁(7.1~7.3) | C. | 胃液(0.9~1.5) | D. | 血浆(7.35~7.45) |