题目内容
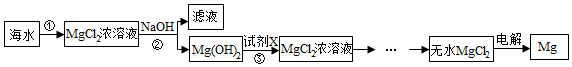
9.镁被誉为“国防金属”,工业上通常用海水制取金属镁,有以下两个方案:方案一:
方案二:
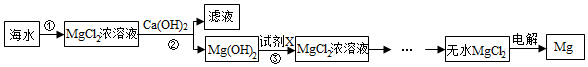
请回答下列问题:
(1)每吨试剂价格表:
| 试剂 | NaOH | Ca(OH)2 |
| 价格(元/t) | 3200 | 1200 |
(2)步骤②中加入试剂充分反应后的操作是过滤;
(3)步骤③发生反应的化学方程式Mg(OH)2+2HCl=MgCl2+2H2O;
(4)在MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑反应中化合价发生变化的元素有2种.
分析 氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,和氢氧化钙反应生成氢氧化镁沉淀和氯化钙;
氢氧化镁和稀盐酸反应生成氯化镁和水.
解答 解:(1)由表中信息可知,氢氧化钙价格低于氢氧化钠,因此工业生产为了获得更高的利润,最好选择方案二.
故填:二.
(2)步骤②中加入试剂充分反应后的操作是过滤,通过过滤把液体和固体分离.
故填:过滤.
(3)步骤③中氢氧化镁和稀盐酸反应生成氯化镁和水,发生反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O.
故填:Mg(OH)2+2HCl=MgCl2+2H2O.
(4)在MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑反应中,反应前镁元素化合价是+2,反应后是0,反应前氯元素化合价是-1,反应后是0,因此化合价发生变化的元素有2种.
故填:2.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
13.下列各组物质能同时存在一瓶水溶液中,且溶液为无色的是( )
| A. | Na2CO3、NaCl | B. | KCl、Fe(NO3)3 | C. | H2SO4、BaCl2 | D. | KNO3、CuSO4 |
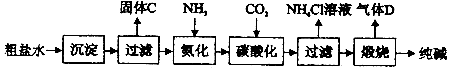
17.我国化学家侯徳榜的“联合制碱法”工艺简洁效率高.其主要反应如下:
①NH3+H2O+CO2═NH4HCO3
②NaCl(饱和)+NH4HCO3═NH4C1+NaHCO3↓
③2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
下列说法正确的是( )
①NH3+H2O+CO2═NH4HCO3
②NaCl(饱和)+NH4HCO3═NH4C1+NaHCO3↓
③2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
下列说法正确的是( )
| A. | ②反应是复分解反应 | |
| B. | ③反应过程中碳元素的化合价发生了改变 | |
| C. | ③反应后的H2O和CO2可以被循环使用 | |
| D. | 反应结束后,只得到一种产物Na2CO3 |
14.考古学家通过测定文物遗骸中的碳-14含量来推断文物年代.碳-14原子的核电荷数为6,相对原子质量为14.下列关于碳-14原子的说法中,错误的是( )
| A. | 中子数为14 | B. | 质子数为6 | ||
| C. | 电子数为6 | D. | 质子数和中子数值之和为14 |
1.下列四位同学分别设计的实验方案,你认为不可行的是( )
| A. | 将pH试纸湿润后,用玻璃棒蘸取食用白醋滴到试纸上,测定其pH | |
| B. | 确定某溶液中是否含有硫酸根离子,可先向该溶液中滴加稀盐酸,若没有任何明显现象,则继续滴加氯化钡溶液,然后观察是否有白色沉淀生成 | |
| C. | 通过灼烧、闻燃烧产生的气味可以鉴别合成纤维与羊毛纤维 | |
| D. | 通过足量灼热的铜网可以除去氮气中混有的少量氧气 |
18.下列实验操作或装置错误的是( )
| A. |  实验室制取二氧化碳 | B. |  向试管中滴加溶液 | ||
| C. |  检查装置的气密性 | D. |  实验室制取氧气 |