题目内容
4.工业用石灰石吸收废气中的二氧化硫,并制取石膏(主要成分为硫酸钙),简易流程如图,主要的反应为:2CaCO3+O2+2SO2═2CaSO4+2X.
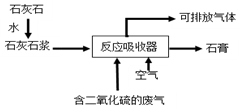
(1)主要反应中物质X的化学式为:CO2.
(2)反应前后,硫元素化合价从+4→+6.
(3)减少二氧化硫的排放,主要为了A.(填序号)
A.减少酸雨形成 B.减少温室效应 C.防止破坏臭氧层
(4)若处理含有3.2kg二氧化硫的废气,要将其完全吸收,至少需要碳酸钙5kg.
分析 化学反应前后,元素的种类不变,原子的种类、总个数和质量不变;
化合物中元素化合价代数和为零,单质中元素化合价规定为零;
二氧化硫、二氧化氮等物质是导致酸雨的重要物质;
根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)由2CaCO3+O2+2SO2═2CaSO4+2X可知,反应前后钙原子都是2个,硫原子都是2个,反应前碳原子是2个,反应后应该是2个,包含在2X中,反应前氧原子是12个,反应后应该是12个,其中4个包含在2X中,因此主要反应中物质X的化学式为CO2.
故填:CO2.
(2)根据化合物中元素化合价代数和为零可知,二氧化硫中硫元素的化合价是+4,硫酸钙中硫元素的化合价是+6,因此反应前后,硫元素化合价从+4→+6.
故填:+6.
(3)减少二氧化硫的排放,主要为了减少酸雨形成.
故选:A.
(4)设至少需要碳酸钙质量为x,
2CaCO3+O2+2SO2═2CaSO4+2CO2,
200 128
x 3.2kg
$\frac{200}{x}$=$\frac{128}{3.2kg}$,
x=5kg,
答:至少需要碳酸钙质量是5kg.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
14.某课外活动小组的同学在测定由氯化钠和碳酸钠形成的固体混合物组成时.进行了以下实验:取80g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的氯化钙溶液,实验数据见表.计算:
(1)加入氯化钙溶液的质量分数;
(2)原固体混合物中碳酸钠的质量分数.
| 实验 | 1 | 2 | 3 | 5 |
| 原固体混合物质量/g | 20 | 20 | 20 | 20 |
| 加入氯化钙溶液质量/g | 20 | 40 | 60 | 80 |
| 生成的沉淀质量/g | 4 | 8 | 10 | 10 |
(2)原固体混合物中碳酸钠的质量分数.
19. 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是( )
 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是( )| 甲 | 乙 | |
| A | 稀硫酸和铜片 | 水和硝酸铵固体 |
| B | Na2CO3溶液和稀硫酸 | 水和浓硫酸 |
| C | 双氧水和MnO2 | NaOH溶液和CO2 |
| D | 水和氢氧化钠固体 | AgNO3溶液和稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
16.“芒果花开,香气扑面”的现象说明( )
| A. | 分子之间有间隔 | B. | 分子的体积很小 | ||
| C. | 分子在不断地运动 | D. | 分子的质量很小 |
13.2017年1月27日,南京理工大学胡炳成教授团队成功合成世界首个全氮阴离子盐(N3-),全氮类超高含能材料(炸药)的能量可达3倍TNT以上(爆炸产物为氮气).下列说法中不正确的是( )
| A. | N3-是氮元素的一种新单质 | |
| B. | N3-是带一个单位负电荷的阴离子 | |
| C. | 全氮类超高含能材料爆炸的产物无污染 | |
| D. | 氮气的化学性质很稳定 |
14.下列是几种粒子的结构示意图,有关说法不正确的是( )

| A. | ②属于稀有气体元素 | B. | ①和②属同种元素 | ||
| C. | ①和③的化学性质相似 | D. | ④属于金属元素 |