题目内容
16.过氧化钙晶体(CaO2•8H2O)较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒.以贝壳为原料制备CaO2流程如下: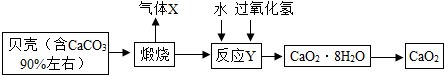
(1)气体X是CO2,其名称是二氧化碳;将过氧化钙晶体与溶液分离的方法是过滤.
(2)反应Y需控制温度在0~5℃,可将反应容器放在冰水混合物中,该反应是化合反应,反应产物是CaO2•8H2O,请写出化学方程式CaO+H2O2+7H2O=CaO2•8H2O.获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是CaO或Ca(OH)2过量,且Ca(OH)2微溶.
(3)CaO2的相对分子质量为72,过氧化钙晶体(CaO2•8H2O)中H、O元素的质量比为1:10.
(4)为测定制得的过氧化钙晶体中CaO2•8H2O的质量分数,设计的实验如下:称取晶体样品50g,加热到220℃充分反应(方程式为2CaO2•8H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CaO+O2↑+16H2O↑,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2•8H2O的质量分数(CaO2•8H2O相对分子质量为216),写出必要的计算过程.
分析 (1)根据化合物的名称以及分离固体与液体的方法来分析;
(2)根据反应需要的温度以及反应的过程来分析;
(3)根据相对分子质量和元素质量比的计算方法来分析;
(4)根据氧气的质量,利用化学方程式进行计算.
解答 解:(1)根据氧化物的命名方法可知,CO2读作二氧化碳;分离固体与液体采用过滤的方法;故填:二氧化碳;过滤;
(2)控制温度在0~5℃,可以在冰水混合物中进行;该反应的反应物是氧化钙、水和过氧化氢,生成物是CaO2•8H2O,因为氧化钙能与水反应生成氢氧化钙,而氢氧化钙微溶于水;故填:冰水混合物;CaO+H2O2+7H2O=CaO2•8H2O;CaO或Ca(OH)2过量,且Ca(OH)2微溶;
(3)CaO2的相对分子质量为40+16×2=72;过氧化钙晶体(CaO2•8H2O)中H、O元素的质量比为(1×16):(16×10)=1:10;故填:72;1:10;
(4)解:设样品中CaO2•8H2O的质量为x
2CaO2•8H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CaO+O2↑+16H2O↑
432 32
x 3.2g
$\frac{432}{32}=\frac{x}{3.2g}$
x=43.2g
则样品中CaO2•8H2O的质量分数为$\frac{43.2g}{50g}×100%$=86.4%
答:样品中CaO2•8H2O的质量分数为86.4%.
点评 本题注意考查化学方程式的书写样品纯度的求算,完成此题,可以依据题干提供的信息进行,书写方程式要注意配平.

练习册系列答案
相关题目
6.人体缺乏必需的元素易患疾病,下列说法正确的是( )
| A. | 缺铁易引起贫血 | B. | 缺氟会引起甲状腺肿大 | ||
| C. | 青少年预防佝偻病,应适量补锌 | D. | 碘元素摄入量不足易患骨质疏松症 |
7.某反应的微观示意图如图,有关说法错误的是( )


| A. | 甲的化学式为NH3 | B. | 该反应是置换反应 | ||
| C. | 丙、丁属于氧化物 | D. | 化学反应前后分子种类发生了变化 |
11.元素周期表中,同周期元素的结构和性质呈现一定的规律性变化.下表列出的是第三周期元素的原子半径及主要化合价(部分信息未列出).下列有关说法不正确的是( )
| 元素 | Na | Mg | ① | Si | P | ② | Cl |
| 原子的最外层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 原子半径(10-10m) | 1.86 | 1.60 | 1.43 | ③ | 1.10 | 1.02 | 0.994 |
| 最高正价 最低负价 | +1 | +2 | ④ | +4 -4 | +5 -3 | ⑤ | +7 -1 |
| A. | ⑤处的最高正价是+6,最低负价是-2 | |
| B. | ③处的数值介于1.10-1.43之间 | |
| C. | 第三周期元素(Na-Cl)的最高正价数等于其原子的最外层电子数 | |
| D. | 元素①的原子序数是13,①和②形成的化合物的化学式为AlS |
1.下列变化中属于化学变化的是( )
| A. | 滴水成冰 | B. | 铁杵成针 | C. | 热胀冷缩 | D. | 百炼成钢 |
8.下列物质中,不属于糖类的是( )
| A. | 葡萄糖 | B. | 淀粉 | C. | 蛋白质 | D. | 纤维素 |
5.下列各组变化中,每个转化在一定条件下均能一步实现的是( )


| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
 某补钙药剂说明书的部分信息如图所示,现将用20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应后称得剩余物的质量为55.6g,请回答下列问题(计算请写出过程):
某补钙药剂说明书的部分信息如图所示,现将用20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应后称得剩余物的质量为55.6g,请回答下列问题(计算请写出过程):