题目内容
7.以下是金属锡纯度的一种测定方法:步骤i 将样品全部溶于盐酸生成SnCl2溶液;
步骤ii 往所得SnCl2溶液加入过量的FeCl3溶液,发生反应:
SnCl2+2FeCl3═SnCl4+2FeCl2
步骤iii 用K2Cr2O7溶液测定步骤ii反应生成FeCl2的质量.
现有金属锡样品1.20g,经上述方法测得生成的FeCl2质量为2.54g(假设杂质不参加反应),计算并回答:
(1)样品溶于盐酸生成的SnCl2质量;
(2)样品中锡的质量分数(精确到0.01%)
分析 (1)根据FeCl2质量计算SnCl2质量;
(2)根据化学方程式利用SnCl2质量计算Sn的质量,进而计算样品中锡的质量分数.
解答 解:设生成的SnCl2质量为x,锡的质量为y
由Sn+2HCl=SnCl2+H2↑,SnCl2+2FeCl3═SnCl4+2FeCl2
则:Sn~~SnCl2~~2FeCl2
119 190 254
y x 2.54g
$\frac{119}{y}=\frac{190}{x}=\frac{254}{2.54g}$
x=1.9g,y=1.19g
(1)样品溶于盐酸生成的SnCl2质量为1.9g;
(2)样品中锡的质量分数:$\frac{1.19g}{1.20g}×100%$=99.17%
答:样品中锡的质量分数为99.17%.
点评 本题属于信息计算题,学生应利用给出的反应来分析反应类型、物质的化学式,并利用多个反应来寻找物质的质量之间的关系式来计算.

练习册系列答案
相关题目
17.化学课上,老师带来一包白色粉末状漂白剂进行探究.老师介绍它可能是双氧水(H2O2)、过氧碳酸钠和过氧化钙(CaO2)中的一种.
【提出猜想】小科认为该漂白剂肯定不是双氧水,他的理由是双氧水常温下是液态;
【查阅资料】
(1)过氧碳酸钠是一种白色结晶颗粒,易溶于水,并与水反应生成碳酸钠和过氧化氢;
(2)过氧化钙,白色固体,极微溶于水,与水反应缓慢释放氧气,同时生成氢氧化钙,反应的化学方程式为2CaO2+2H2O=2Ca(OH)2+O2↑;
【实验验证】同学们设计了下列实验方案进行验证,请将方案的空格填写完整.
【交流反思】
(1)小刚认为只根据操作①便可确定白色固体的成分,理由是溶液浑浊,说明该漂白剂难溶于水,而过氧化钙难溶于水,过碳酸钠能溶于水,说明该漂白剂是过氧化钙;
(2)小强欲验证该漂白剂与水反应生成的气体为氧气,他的实验方法为取漂白剂于试管中加入适量水,并加入二氧化锰,将带火星的木条伸入试管中若木条复燃,证明该气体是氧气.
【提出猜想】小科认为该漂白剂肯定不是双氧水,他的理由是双氧水常温下是液态;
【查阅资料】
(1)过氧碳酸钠是一种白色结晶颗粒,易溶于水,并与水反应生成碳酸钠和过氧化氢;
(2)过氧化钙,白色固体,极微溶于水,与水反应缓慢释放氧气,同时生成氢氧化钙,反应的化学方程式为2CaO2+2H2O=2Ca(OH)2+O2↑;
【实验验证】同学们设计了下列实验方案进行验证,请将方案的空格填写完整.
| 实验内容 | 实验现象 | 实验结论或解释 |
| ①取3g白色固体放入试管中,加入50ml水中,充分振荡 | 液体浑浊 | \ |
| ②小吴另取少量操作①中的上层清液于试管中,通入二氧化碳 | 有白色沉淀产生 | 该漂白剂的成分是过氧化钙 |
(1)小刚认为只根据操作①便可确定白色固体的成分,理由是溶液浑浊,说明该漂白剂难溶于水,而过氧化钙难溶于水,过碳酸钠能溶于水,说明该漂白剂是过氧化钙;
(2)小强欲验证该漂白剂与水反应生成的气体为氧气,他的实验方法为取漂白剂于试管中加入适量水,并加入二氧化锰,将带火星的木条伸入试管中若木条复燃,证明该气体是氧气.
18.下列有关溶液的说法正确的是( )
| A. | 溶液均是无色的、透明的 | |
| B. | 可溶性物质溶于水时一定会放出热量 | |
| C. | 石灰水的溶质是石灰 | |
| D. | 溶液的均一性是指同一溶液各部分的性质、组成相同 |
15.端午节吃粽子是我国的传统习俗,闽南特色粽子的主要原料为大米、肉、海蛎干、食盐,主要原料中富含糖类物质的是( )
| A. | 肉 | B. | 大米 | C. | 食盐 | D. | 海蛎干 |
2. 三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )
三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )
 三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )
三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )| A. | 反应中CaO为催化剂 | B. | 该反应是复分解反应 | ||
| C. | 反应后容器中固体质量减少 | D. | 反应后容器中氧元素质量分数增大 |
12.切洋葱时人会流眼泪,原因是洋葱中含有强烈刺激性的物质正丙硫醇,从分子性质的角度解释,这是利用( )
| A. | 分子很小 | B. | 分子在不断的运动 | ||
| C. | 分子之间有间隔 | D. | 分子可以再分 |
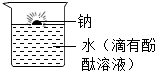 充有的蒸汽的高压钠灯发出的黄光射程远,透雾能力强,常用于道路和广场的照明.钠的化学性质活泼,常温下可以与氧气、水反应,在实验室里,金属钠保存在煤油中,用镊子从煤油中取出金属钠,放在滤纸上,用小刀切下一小块,投入盛有水(滴有酚酞溶液)的烧杯中,发现钠块浮在水面上,很快熔化成银白色小球,四处游动,发出嘶嘶的响声,偶有火星出现,溶液变成红色.依据提供的信息,回答下列问题.
充有的蒸汽的高压钠灯发出的黄光射程远,透雾能力强,常用于道路和广场的照明.钠的化学性质活泼,常温下可以与氧气、水反应,在实验室里,金属钠保存在煤油中,用镊子从煤油中取出金属钠,放在滤纸上,用小刀切下一小块,投入盛有水(滴有酚酞溶液)的烧杯中,发现钠块浮在水面上,很快熔化成银白色小球,四处游动,发出嘶嘶的响声,偶有火星出现,溶液变成红色.依据提供的信息,回答下列问题.