题目内容
15.一个密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得数据见表.下列说法中正确的是( )| 物质质量 | 甲 | 乙 | 丙 | 丁 |
| 反应前 | 25g | x | 5g | 5g |
| 反应后 | 8g | 23g | 5g | 8g |
| A. | x=9g | |
| B. | 该反应是化合反应 | |
| C. | 在该反应中,丙物质一定做催化剂 | |
| D. | 在该反应中甲、乙、丁三种物质的质量比是8:23:8 |
分析 首先根据质量守恒定律:反应前物质的总质量=反应后物质的总质量求出x的数值.然后根据甲、乙、丙、丁四种物质反应前后质量的变化确定出反应物和生成物(即反应后质量增加的为生成物,反应后质量减少的为反应物.),进而判断出该反应的类型.丙物质反应前后质量不变,可能是催化剂或者是没有参加反应进行分析.
解答 解:A、根据质量守恒定律:反应前物质的总质量=反应后物质的总质量可知25+x+5+5=8+23+5+8,x=9g,故A正确;
B、根据甲、乙、丙、丁四种物质反应前后质量的变化可知甲为反应物,乙、丁为生成物,故该反应为:甲→乙+丁,故B错误;
C、丙物质反应前后质量没有变化,该物质可能没有参加反应或者是该反应的催化剂,故C错误;
D、在该反应中甲、乙、丁三种物质的质量比是(25g-8g):(23g-9g):(8g-5g)=13:12:3,故D错误.
故选:A.
点评 该题要求学生要掌握好质量守恒定律并能灵活的加以运用,还要求学生具有会从图表中挖掘出有效数据进行处理的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.我们吃到的味道鲜美的鱼,是这样烹饪出来的:将洗净的鱼煎过后,再加入少许食醋、料酒、生姜、葱、食盐等加热.共热时发生了许多化学反应.其中,食醋中的乙酸(CH3COOH)与料酒中的乙醇(C2H5OH)发生化学反应,生成了有特殊香味的乙酸乙酯(CH3COOC2H5),下列有关说法正确的是( )
| A. | 乙酸乙酯是一种混合物 | |
| B. | 乙酸乙酯是由碳、氢、氧三种元素组成的 | |
| C. | 乙醇中碳、氢、氧三种元素的质量比为2:4:1 | |
| D. | 乙酸乙酯中只有氧元素显负价 |
10.有一在空气中暴露过的KOH固体,经分析测知含H2O 3.12%,K2CO3 6%,其余为KOH.取此样品m g溶于100g 98%的硫酸里,残酸需加 n g KOH才刚好中和完全.由此可知蒸发中和后的溶液可得到多少克固体?( )
| A. | 14.2mg | B. | 174g | C. | $\frac{174(m+n)}{56}$ g | D. | 无法计算 |
20.要除去密闭容器中空气里的氧气,得到较纯净的氮气,可用物质在密闭容器中燃烧的方法,则该被选用的可燃性物质是( )
| A. | 硫 | B. | 木炭 | C. | 红磷 | D. | 蜡烛 |
7.K2SO4是一种重要的钾肥,其中的钾指的是( )
| A. | 钾原子 | B. | 钾离子 | C. | 钾分子 | D. | 钾元素 |
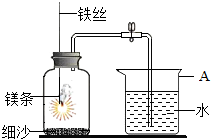 某校研究性学习小组探究空气中氧气的体积分数,他们想选用以下药品进行实验:①木炭;②红磷;③铁丝;④镁条.
某校研究性学习小组探究空气中氧气的体积分数,他们想选用以下药品进行实验:①木炭;②红磷;③铁丝;④镁条.