题目内容
16.测得100g某不纯的硝酸铵(NH4NO3)样品中氮元素质量分数为34.3%,已知杂质中不含氮元素,求:(1)该样品中含氮元素的质量为34.3g.
(2)该样品中硝酸铵的质量分数是多少?(写出计算过程)
分析 (1)根据总质量×氮元素质量分数=氮元素的质量进行解答;
(2)先计算出纯净硝酸铵中氮元素的质量分数,再计算样品中NH4NO3的质量分数(即纯度),依据纯度=含杂质物质元素的质量分数÷物质中某元素的质量分数,进行解答.
解答 解:(1)34.3g;
故答案是:34.3g;
(2)设样品中硝酸铵的质量为x,
则100g×34.3%=x×$\frac{28}{80}$×100%,
解得x=98g.
硝酸铵的质量分数为:$\frac{98g}{100g}$×100%=98%.
答:样品中硝酸铵的质量分数是98%.(或其他合理解题过程均可酌情给分).
点评 将质量分数的计算与生活实际相联系;计算时要理清各个量之间的关系,再结合题意进行分析解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.小芳在上化学课时听老师讲,水垢可以用稀盐酸或食醋除去.回到家中她发现家里的水壶底部有水垢,于是取将家里的“保宁”牌醋倒了些在水壶中,发现有大量气泡产生.第二天小芳到学校向老师的告这一现象,并问老师水垢和醋反应生成的气体是什么.老师告诉小芳,这种气体是水垢(主要成份是CaCO3)与醋酸(CH3COOH)反应生成的,并建议她做实验对这一问题进行探究.于是小芳约了小明、小华一起到实验实进行探究,请你和他们一起完成这次有趣的探究活动.
【提出问题】水垢和醋酸反应生成的气体是什么?
【猜想】小芳的猜想:这种气体是氧气;
小明的猜想:这种气体是氮气;
小华的猜想:这种气体是二氧化碳;
在讨论中小华和小芳一致认为小明的猜想是错误的,他们的理由是由质量守恒定律可知,水垢(主要成份是CaCO3)与醋酸(CH3COOH)只含有C、H、O、Ca四种元素,不可能生成含氮元素的氮气;
【进行实验室】小芳和小华各自进行实验,验证自己的猜想是否正确.请你和小华一起完成下列探究报告.
【提出问题】水垢和醋酸反应生成的气体是什么?
【猜想】小芳的猜想:这种气体是氧气;
小明的猜想:这种气体是氮气;
小华的猜想:这种气体是二氧化碳;
在讨论中小华和小芳一致认为小明的猜想是错误的,他们的理由是由质量守恒定律可知,水垢(主要成份是CaCO3)与醋酸(CH3COOH)只含有C、H、O、Ca四种元素,不可能生成含氮元素的氮气;
【进行实验室】小芳和小华各自进行实验,验证自己的猜想是否正确.请你和小华一起完成下列探究报告.
| 操作内容 | 实验现象 | 结论 |
| ①取少量水垢放入试管中,加入适量醋酸; ②将涂有少量石灰水的玻璃片放在试管口. | ①有大量气泡冒出 ②澄清的石灰水变浑浊 | 小华的猜想正确. |
11.以下是一个化学反应的微观示意图,从示意图中获取的信息不正确的是( )
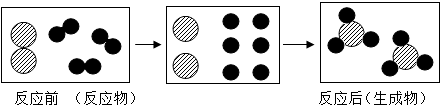

| A. | 分子在化学反应中可分为原子 | |
| B. | 反应前后同种元素的质量发生了改变 | |
| C. | 化学反应前后原子的种类不变 | |
| D. | 反应后分子不再保持反应前分子的化学性质 |
1.下列事实的结论或解释中不正确的是( )
| A. | 水烧开后易把壶盖冲起--说明温度升高分子会变大 | |
| B. | 公园的桂花开放时满园飘香--说明分子在不断运动 | |
| C. | 固体很难被压缩--说明分子间间隔小 | |
| D. | 水通电生成氢气和氧气--说明化学反应中分子分为原子,原子组合成新分子 |
5.已知核电荷数的下列各组元素中,能形成XY2型化合物的是( )
| A. | 1和8 | B. | 2和9 | C. | 11和16 | D. | 12和17 |
6.等质量的下列物质,加入等质量的水和稀盐酸,反应后溶液的总质量不会改变的是( )
| A. | Fe | B. | K2CO3 | C. | NaOH | D. | AgNO3 |
 某同学设计了测定空气中氧气含量的实驗.实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实驗.实验装置如图.该同学的实验步骤如下: