题目内容
12.某同学在家做食醋和纯碱的实验:取一定量的食醋于烧杯中向其中加入5.3g纯碱,恰好完全反应后,称得反应后物质的质量为153.1g,则所取食醋的浓度为 ( )| A. | 12% | B. | 4% | C. | 8% | D. | 2% |
分析 根据碳酸钠的质量求出醋酸的质量以及生成二氧化碳的质量,进而求出食醋的质量以及食醋的浓度即可.
解答 解:设食醋中醋酸的质量为x,生成二氧化碳的质量为y,
Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑
106 120 44
5.3g x y
$\frac{106}{5.3g}=\frac{120}{x}=\frac{44}{y}$
x=6.0g
y=2.2g
所取食醋的浓度=$\frac{6.0g}{153.1g+2.2g-5.3g}×100%$=4%
故选:B.
点评 此题是对化学方程式计算的考查题,解题的关键是对反应前后物质的质量之差是二氧化碳质量的分析.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
3.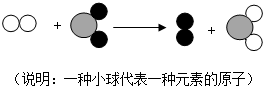 两种物质在一定条件下能发生化学反应,其反应的微观示意图如所示.则下列说法中正确的是( )
两种物质在一定条件下能发生化学反应,其反应的微观示意图如所示.则下列说法中正确的是( )
 两种物质在一定条件下能发生化学反应,其反应的微观示意图如所示.则下列说法中正确的是( )
两种物质在一定条件下能发生化学反应,其反应的微观示意图如所示.则下列说法中正确的是( )| A. | 该反应中反应物和生成物都是化合物 | |
| B. | 该图示体现的是置换反应 | |
| C. | 化学反应前后分子和原子种类都不变 | |
| D. | 该反应中,参加反应的两种物质分子数之比是1:2 |
17.化学反应方程式书写正确的是( )
| A. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2 | B. | 6HCl+2Fe=2FeCl3+3H2↑ | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | 2KClO3=2KCl+3O2↑ |
4.分类是学习和研究化学的常用方法.下列分类中正确的是( )
| A. | 合成材料:合金、合成橡胶、合成纤维 | |
| B. | 有机物:甲烷、乙醇、葡萄糖(C6H12O6) | |
| C. | 混合物:煤、石油、冰水共存物 | |
| D. | 复合肥料:尿素、硝酸钾、磷酸氢二铵 |
1.现有银、铁、铜三种金属丝,为探究它们的金属活动性顺序,某同学设计了如下实验方案,请你根据他记录的相关信息,回答下列问题:
(1)填写下表“实验现象”
(2)三种金属的活动性由强到弱的顺序是Fe>Cu>Ag.
(3)写出铁与稀硫酸反应的化学方程式Fe+H2SO4═FeSO4+H2↑.
(4)要比较以上三种金属的活动性顺序还可以选择以下哪组试剂A.
A.铁、硫酸铜溶液、银 B.铁、铜、硝酸银溶液
C.硫酸亚铁溶液、铜、银 D.硫酸亚铁溶液、硫酸铜溶液、银.
(1)填写下表“实验现象”
| 序号 | 实验步骤 | 实验现象 |
| 1 | 取铁丝浸入稀硫酸中 | 产生气泡,溶液由无色变浅绿色 |
| 2 | 取铜丝浸入稀硫酸中 | 无现象 |
| 3 | 取银丝浸入硫酸铜溶液中 | 无现象 |
(3)写出铁与稀硫酸反应的化学方程式Fe+H2SO4═FeSO4+H2↑.
(4)要比较以上三种金属的活动性顺序还可以选择以下哪组试剂A.
A.铁、硫酸铜溶液、银 B.铁、铜、硝酸银溶液
C.硫酸亚铁溶液、铜、银 D.硫酸亚铁溶液、硫酸铜溶液、银.
2.甲、乙、丙、丁四种化合物,均由Na、S、O、H中的2种或3种元素组成.它们可发生如下反应:
甲+Ba(NO3)2→盐+盐 乙+NaOH→盐+水
丙+HCl→盐+水 丁+CaO(或CO2)→碱(或酸).
下列判断正确的是( )
甲+Ba(NO3)2→盐+盐 乙+NaOH→盐+水
丙+HCl→盐+水 丁+CaO(或CO2)→碱(或酸).
下列判断正确的是( )
| A. | 甲可能是Na2SO4,乙一定是H2SO4 | B. | 乙可能是H2SO4,丙一定是NaOH | ||
| C. | 甲可能是NaHSO4,丙一定是NaOH | D. | 乙可能是H2SO4,丁一定是H2O |
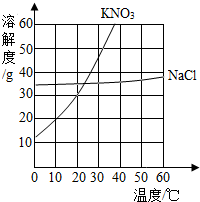 如图是KNO3和NaCl的溶解度曲线,回答下列问题.
如图是KNO3和NaCl的溶解度曲线,回答下列问题.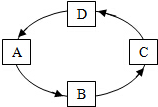 已知A、B、C、D均为初中化学中最常见的物质,它们之间存在如图所示的转化关系,其中A为最常见的溶剂.
已知A、B、C、D均为初中化学中最常见的物质,它们之间存在如图所示的转化关系,其中A为最常见的溶剂.