题目内容
7.某学习小组的同学们设计了三种制取氯化钙溶液的实验方法,这三种方法都选用了稀盐酸和一种物质发生反应.(1)请你填写他们设计的三种方法中的另一种反应物.
方法Ⅰ:用稀盐酸跟氢氧化钙反应;
方法Ⅱ:用稀盐酸跟碳酸钙反应;
方法Ⅲ:用稀盐酸跟氧化钙反应.
(2)写出你填写的方法Ⅰ所发生反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
分析 根据性质结合复分解反应的条件来分析用稀盐酸和一种物质发生反应制取氯化钙的方法.
解答 解:(1)方法Ⅰ:可以用稀盐酸跟氢氧化钙反应生成氯化钙和水;
方法Ⅱ:可以用稀盐酸跟碳酸钙反应生成氯化钙和水和二氧化碳;
方法Ⅲ:可以用稀盐酸跟氧化钙反应生成氯化钙和水;
(2)用稀盐酸跟氢氧化钙反应生成氯化钙和水;Ca(OH)2+2HCl═CaCl2+2H2O;
答案:(1)氢氧化钙;碳酸钙;氧化钙;
(2)Ca(OH)2+2HCl═CaCl2+2H2O.
点评 本题难度不大,考查学生对酸的性质的掌握和复分解反应的条件的理解和运用,根据反应原理书写化学方程式的能力.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
3.下列有关分子、原子和离子的说法正确的是( )
| A. | 分子在化学反应前后保持不变 | |
| B. | 氯化钠是由离子构成的化合物 | |
| C. | 原子的最外层电子数决定元素的种类 | |
| D. | 分子间有一定间隔,原子间没有间隔 |
18.下列化学反应中既是化合反应也是氧化反应的是( )
| A. | 二氧化碳+水→碳酸 | |
| B. | 铜+氧气+二氧化碳+水→碱式碳酸铜 | |
| C. | 石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳 | |
| D. | 高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气 |
2.下列做法中不利于环境保护的是( )
| A. | 工业废水直接排放 | B. | 保护生物多样性 | ||
| C. | 植树造林 | D. | 大量使用农药、化肥 |
19.研究和控制化学反应条件有重要意义.
①同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以制取氧气,同学们可以选择下列图1中的D(选填编号)装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,因此加热不适合用于双氧水制取氧气.
②同学们还想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
Ⅰ. 取用二氧化锰的仪器是图2中的B(选填编号).
Ⅱ.写出上述反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
Ⅲ.本实验中收集氧气选用的装置有CD(选填编号).
Ⅳ.实验2中双氧水溶质质量分数为12%.
Ⅴ.实验3中,加入的二氧化锰质量为5g.
Ⅵ.相同条件下,实验3产生氧气的速率最快,说明在相同的条件下,双氧水的溶质质量分数越大,反应速率越快.
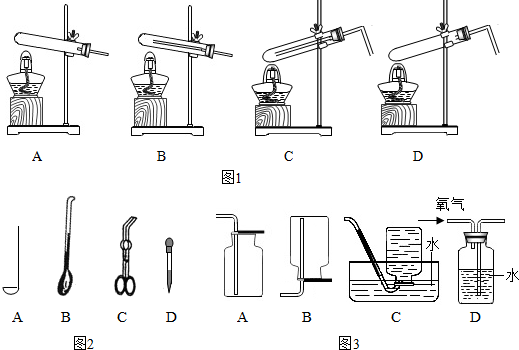
①同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以制取氧气,同学们可以选择下列图1中的D(选填编号)装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,因此加热不适合用于双氧水制取氧气.
②同学们还想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |
Ⅱ.写出上述反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
Ⅲ.本实验中收集氧气选用的装置有CD(选填编号).
Ⅳ.实验2中双氧水溶质质量分数为12%.
Ⅴ.实验3中,加入的二氧化锰质量为5g.
Ⅵ.相同条件下,实验3产生氧气的速率最快,说明在相同的条件下,双氧水的溶质质量分数越大,反应速率越快.

17.不属于碱的物质是( )
| A. | NH3•H2O | B. | Na2CO3 | C. | NaOH | D. | Fe(OH)3 |