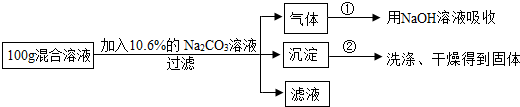
题目内容
13.氢气、木炭、一氧化碳是金属冶炼中常用的还原剂.如图甲是氢气还原氧化铜的实验,如图乙是木炭还原氧化铁的实验,如图丙是一氧化碳还原氧化铜的实验.
(1)实验步骤的先后次序很重要,如甲实验中反应前须先通氢气后点灯,否则易发生爆炸;请再列出二项不能颠倒的先后次序:甲实验中反应后必须先熄灭酒精灯,继续通入H2直至试管冷却,否则生成的红色的铜会变成黑色;丙实验中反应前必须先点尾灯,后通CO,否则易发生煤气中毒.
(2)某同学正确操作做完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,用另一试管取5克黑色残留粉末,加入足量稀硫酸充分振荡,她惊讶地发现试管中并未产生预期的气泡,她向老师求教,才知道“铁的氧化物除了氧化铁和四氧化三铁外还有氧化亚铁(也为黑色),其中只有四氧化三铁常温下不溶于稀硫酸”,于是她又对试管中的悬浊液进行过滤和烘干操作,滤液无色澄清,滤渣经称量后仍为5克.请你据此写出乙实验试管中发生的化学方程式C+6Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$4Fe3O4+CO2↑.
(3)到底是什么原因导致乙实验的冶炼效果不理想呢?该同学先经过科学猜想,后用酒精喷灯代替普通酒精灯重做这个实验来加以验证,结果证明她的猜想是正确的.由此推断,该同学的科学猜想是加热的温度不够高.
分析 (1)根据氢气还原氧化铜的实验顺序和一氧化碳的毒性来分析;
(2)根据题干信息以及化学方程式的书写方法来分析解答.
(3)根据酒精喷灯和普通酒精灯的差异分析.
解答 解:(1)实验结束后,某同学发现试管里红色的物质又变成黑色,原因是灼热的铜和空气反应生成黑色氧化铜,即没有继续通入H2直至试管冷却;
因为一氧化碳有毒,不能直接排到大气中,可以用点燃的方法除去一氧化碳,所以应该先点燃后面的酒精灯,故填:先熄灭酒精灯,继续通入H2直至试管冷却;先点尾灯,后通CO;
(2)因为氧化亚铁能溶于酸,而四氧化三铁不能溶于酸,故黑色固体为四氧化三铁,故填:C+6Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$4Fe3O4+CO2↑.
(3)酒精喷灯比普通酒精灯可以提供更高的温度,所以应该是由于温度不够高导致乙实验的冶炼效果不理想.故填:加热的温度不够高.
点评 本题考查了还原氧化铁的注意事项以及化学方程式的书写,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.酸溶液中都含有H+,因此不同的酸溶液都表现出一些共同的化学性质(即酸的共性).下列关于硫酸性质的表述中不属于酸的共同性质的是( )
| A. | 能使紫色石蕊溶液变红 | B. | 能与氢氧化钠反应生成水 | ||
| C. | 能与CuO反应生成水 | D. | 能与BaCl2溶液反应生成BaSO4沉淀 |
2.下列化学方程式符合题意且书写正确的是( )
| A. | 不能用铁器盛放硫酸铜溶液的原因:Fe+CuSO4═FeSO4+Cu | |
| B. | 工业上用赤铁矿炼铁:Fe2O3+2CO$\frac{\underline{\;高温\;}}{\;}$2Fe+2CO2 | |
| C. | 医疗上用碱性物质治疗胃酸过多:Mg(OH)2+H2SO4═MgSO4+2H2O | |
| D. | 制取少量硫酸铝:2AlCl3+3H2SO4=Al2(SO4)3+6HCl |
 A、B、C、D、E、F都是初中化学常见的物质,它们之间的关系如图所示.(图中“一”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系.)其中:B是常用于光合用的气体,D是一种微溶于水的物质,B与E不含相同元素,D与A含两种相同元素.
A、B、C、D、E、F都是初中化学常见的物质,它们之间的关系如图所示.(图中“一”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系.)其中:B是常用于光合用的气体,D是一种微溶于水的物质,B与E不含相同元素,D与A含两种相同元素.