题目内容
17.从物质的质量变化研究化学反应就可得出质量守恒定律,下列表述正确的是( )| A. | 1个碳原子在1个氧气分子中完全燃烧,生成1个二氧化碳气体分子 | |
| B. | 32g硫与32g氧气完全反应,生成64g二氧化硫 | |
| C. | 镁条燃烧后固体质量增加,故质量守恒定律不是普遍规律 | |
| D. | 根据:蜡烛+氧气$\stackrel{加热}{→}$二氧化碳+水,则蜡烛中一定含有C、H、O三种元素 |
分析 质量守恒定律是指参加化学反应的各物质的质量总和等于生成的各物质的质量总和.这里强调是所有的反应物和所有的生成物的质量是相等的.
解答 解:
A、1个碳原子在1个氧气分子中完全燃烧,生成1个二氧化碳气体分子不能体现质量守恒.不正确;
B、根据硫燃烧的化学方程式中各物质的质量比可知,32g硫与32g氧气完全反应,生成64g二氧化硫.正确;
C、镁燃烧是镁与氧气反应生成氧化镁,应该是生成的氧化镁的质量等于反应掉的镁和氧气的质量的和,所以生成固体的质量大于镁质量是遵循质量守恒定律的.不正确.
D、物质在氧气中燃烧生成二氧化碳和水,由于反应物中出现了氧气,所以对该物质无法判定是否含有氧元素,可以得出的结论是该物质一定含有碳元素和氢元素,可能含有氧元素,而不是一定含有.错误.
故选:B.
点评 所有的化学变化都遵循质量守恒定律,在使用质量守恒定律时,要注意对所有物质的质量变化考虑在内,同时要考虑是否是恰好完全反应.

练习册系列答案
相关题目
8.下列实验操作正确的是( )
| A. |  滴加液体 | B. |  闻气体气味 | C. | 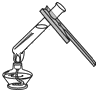 加热液体 | D. |  量9.5mL液体 |
12.下列实验中,可验证物质的化学性质的是( )
| A. |  木炭吸附 | B. |  闻气味 | C. |  石墨导电性 | D. |  纸花变色 |
2.人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属.请回答:
(1)根据如图的应用实例,试说出金属具有的两点物理性质:①导电性;②导热性.

(2)日常使用的金属材料多数属于合金.下表列出了一些常见合金的主要成分和性能.
由上表推断,与组成合金的纯金属相比,合金的优点一般有②④(填序号).
①强度更低②硬度更高③熔点更高④抗腐蚀性更好
(3)铝具有很好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化;随着金属矿产的不断减少,金属的防护已成为世界研究的课题,请你写一条防护金属制品的措施:刷漆.
(4)人们每年要从金属矿物资源中提取数以亿吨计的金属.根据所学化学知识,请写出一个有金属Cu生成的反应的化学方程式:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
(1)根据如图的应用实例,试说出金属具有的两点物理性质:①导电性;②导热性.

(2)日常使用的金属材料多数属于合金.下表列出了一些常见合金的主要成分和性能.
| 合金 | 合金的主要性能 | 主要成分及纯金属的性能 |
| 焊锡 | 熔点183℃ | 锡:熔点232℃;铅:熔点327℃ |
| 硬铝 | 强度和硬度好 | 铝、铜、镁等.硬度小,质软 |
| 不锈钢 | 抗腐蚀性好 | 铁、铬、镍等.纯铁抗腐蚀性能不如不锈钢 |
①强度更低②硬度更高③熔点更高④抗腐蚀性更好
(3)铝具有很好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化;随着金属矿产的不断减少,金属的防护已成为世界研究的课题,请你写一条防护金属制品的措施:刷漆.
(4)人们每年要从金属矿物资源中提取数以亿吨计的金属.根据所学化学知识,请写出一个有金属Cu生成的反应的化学方程式:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
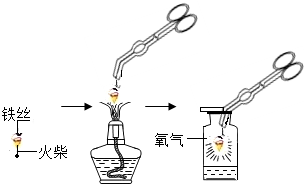 学习了氧气的性质后,小浩和小亮同学想探究铁丝在氧气中燃烧的实验.实验步骤:取几根纱窗细铁丝,擦去表面的铁锈和油漆,拧成一束呈螺旋状绕在一根火柴上,点燃火柴,待火柴临近烧完时缓缓伸入盛氧气的集气瓶中,实验流程如图所示:
学习了氧气的性质后,小浩和小亮同学想探究铁丝在氧气中燃烧的实验.实验步骤:取几根纱窗细铁丝,擦去表面的铁锈和油漆,拧成一束呈螺旋状绕在一根火柴上,点燃火柴,待火柴临近烧完时缓缓伸入盛氧气的集气瓶中,实验流程如图所示:




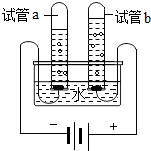 水是人类最宝贵的自然资源,多一滴水,就可能多一条生命.小明利用如图所示的装置探究水的组成.a、b试管内产生的气体分别是氢气、氧气,通电一段时间后,a试管与b试管所收集到的气体体积之比约为2:1,该实验验证了水是由氢元素和氧元素组成的.
水是人类最宝贵的自然资源,多一滴水,就可能多一条生命.小明利用如图所示的装置探究水的组成.a、b试管内产生的气体分别是氢气、氧气,通电一段时间后,a试管与b试管所收集到的气体体积之比约为2:1,该实验验证了水是由氢元素和氧元素组成的.