题目内容
17.下列有关NaOH的实验方案中,正确的是( )| A. | 用NaOH固体干燥CO2气体 | |
| B. | 用酚酞溶液检验NaOH溶液是否变质 | |
| C. | 用熟石灰和纯碱为原料制取NaOH | |
| D. | 用CaCl2溶液除去NaOH溶液中的少量Na2CO3 |
分析 A、根据氢氧化钠溶液会与二氧化碳反应进行分析;
B、根据氢氧化钠、碳酸钠都显碱性,都能使酚酞变红色进行分析;
C、根据氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠进行分析;
D、根据氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠进行分析.
解答 解:A、氢氧化钠溶液会与二氧化碳反应,二氧化碳是酸性气体,不能用碱性干燥剂干燥,故A错误;
B、氢氧化钠、碳酸钠都显碱性,都能使酚酞变红色,故B错误;
C、氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故C正确;
D、氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,生成的氯化钠对于氢氧化钠也是杂质,故D错误.
故选:C.
点评 此题是一道实验方案评价题,解题的关键是能对相关的化学反应有一个较清晰的认识,属基础性知识考查题.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案
相关题目
7.本着“低碳生活.生态文明“的理念,安徽力争在2017年实现全省16市覆盖公共自行车.下列做法不符合该理念的是( )
| A. | 垃圾分类回收、利用 | B. | 汽车使用催化净化装置 | ||
| C. | 大量使用一次性塑料袋 | D. | 开发利用新型能源 |
8. 青铜是铜锡合金,某学习小组为研究其中锡(Sn,银白色金属)和铜的活动性顺序,进行了如下的探究
青铜是铜锡合金,某学习小组为研究其中锡(Sn,银白色金属)和铜的活动性顺序,进行了如下的探究
探究一:金属锡和铜的活动性顺序
若在生成物中锡元素为+2价,则该反应的化学方程式为Sn+CuSO4=SnSO4+Cu.
实验过程中,小组同学还发现试管中有无色气体产生,于是继续探究.
探究二:无色气体的成分
【猜想假设】A、氢气 B、氧气 C、二氧化硫 D、二氧化碳 E、一氧化碳
【分析推理】小明认为无色气体不可能是二氧化碳或一氧化碳,理由是反应物中不含碳元素,化学反应前后元素种类不变.
【查阅资料】二氧化硫能溶于水,且水溶液呈酸性
【设计方案】(1)依据资料,小红设计如表实验
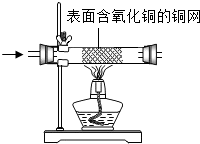
(2)为确定气体成分,小组同学将气体通入如图所示装置,装置中表面含氧化铜的铜网由黑色变为光亮的红色
【得出结论】锡与硫酸铜溶液反应时,产生的气体是氢气.
【思维拓展】
(1)由上述实验可以推出,硫酸铜溶液中可能含有酸.
(2)影响气体生成的快慢的因素有哪些、列出其中一种因素,并设计实验验证.在常温下,取两份大小、形状、纯度相同的锡片,分别加入相同体积但不同的浓度的硫酸铜溶液来进行实验,然后测量收集相同体积的气体所需的时间,从而得出结论.
 青铜是铜锡合金,某学习小组为研究其中锡(Sn,银白色金属)和铜的活动性顺序,进行了如下的探究
青铜是铜锡合金,某学习小组为研究其中锡(Sn,银白色金属)和铜的活动性顺序,进行了如下的探究探究一:金属锡和铜的活动性顺序
| 实验方案 | 实验现象 | 实验结论 |
| 将金属锡加入盛有硫酸铜溶液的试管中 | 在锡表面会有红色的物质生成 | 锡比铜的金属活动性强 |
实验过程中,小组同学还发现试管中有无色气体产生,于是继续探究.
探究二:无色气体的成分
【猜想假设】A、氢气 B、氧气 C、二氧化硫 D、二氧化碳 E、一氧化碳
【分析推理】小明认为无色气体不可能是二氧化碳或一氧化碳,理由是反应物中不含碳元素,化学反应前后元素种类不变.
【查阅资料】二氧化硫能溶于水,且水溶液呈酸性
【设计方案】(1)依据资料,小红设计如表实验
| 实验方案 | 实验现象 | 实验结论 |
| 将收集到到气体通入紫色石蕊试液中 | 紫色石蕊溶液不变色 | 无色气体不是二氧化硫 |
【得出结论】锡与硫酸铜溶液反应时,产生的气体是氢气.
【思维拓展】
(1)由上述实验可以推出,硫酸铜溶液中可能含有酸.
(2)影响气体生成的快慢的因素有哪些、列出其中一种因素,并设计实验验证.在常温下,取两份大小、形状、纯度相同的锡片,分别加入相同体积但不同的浓度的硫酸铜溶液来进行实验,然后测量收集相同体积的气体所需的时间,从而得出结论.
12.青蒿素(化学式C15H22O5)是中国科学家从植物中成功分离出的抗疟药的有效成分,它属于( )
| A. | 单质 | B. | 纯净物 | C. | 氧化物 | D. | 混合物 |
9.下列做法正确的是( )
| A. | 煤气泄漏,开灯检查 | B. | 食品防腐,甲醛浸泡 | ||
| C. | 限放鞭炮,保护环境 | D. | 深埋电池,消除污染 |
4.实验室常用的制取气体的发生装置如图:

(1)仪器a的名称是试管;搭建B装置时,酒精灯应在固定仪器a之前(选填“前”或“后”)放置.
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)在实验室制取二氧化碳的研究中,进行了如下实验:
①上述实验中反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.
②若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号).
③除盐酸的浓度外,上述实验研究的另一个影响反应的因素是固体反应物的颗粒大小(或反应物的接触面积).
④研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是AB(选填编号)
A、反应更为剧烈 B、最终剩余溶液的质量更小
C、产生的二氧化碳的质量更大 D、粉末状大理石利用率更高.

(1)仪器a的名称是试管;搭建B装置时,酒精灯应在固定仪器a之前(选填“前”或“后”)放置.
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)在实验室制取二氧化碳的研究中,进行了如下实验:
| 药品 实验编号 | 甲 | 乙 | 丙 | 丁 |
| 大理石 | m g,块状 | m g,块状 | m g,粉末状 | m g,粉末状 |
| 盐酸(过量) | w g,稀盐酸 | w g,浓盐酸 | w g,稀盐酸 | w g,浓盐酸 |
②若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号).
③除盐酸的浓度外,上述实验研究的另一个影响反应的因素是固体反应物的颗粒大小(或反应物的接触面积).
④研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是AB(选填编号)
A、反应更为剧烈 B、最终剩余溶液的质量更小
C、产生的二氧化碳的质量更大 D、粉末状大理石利用率更高.

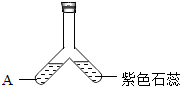 如图所示装置中观察到紫色石蕊变红.
如图所示装置中观察到紫色石蕊变红.