题目内容
7.本着“低碳生活.生态文明“的理念,安徽力争在2017年实现全省16市覆盖公共自行车.下列做法不符合该理念的是( )| A. | 垃圾分类回收、利用 | B. | 汽车使用催化净化装置 | ||
| C. | 大量使用一次性塑料袋 | D. | 开发利用新型能源 |
分析 根据绿色环保进行分析,绿色环保指的是生活作息时所耗用的能量要尽量减少,减少污染物的排放,特别是减少二氧化碳的排放量,防止环境污染,减缓生态恶化等,根据是否能达到这一理念进行分析判断.
解答 解:A、分类回收、利用垃圾,减少资源浪费,能废物利用,符合理念;
B、使用催化净化装置,减少汽车尾气污染,防止空气的污染.符合理念;
C、大量使用一次性塑料袋,会造成大量的白色污染,不符合理念;
D、开发利用新型能源,减少化石使用燃料,节约能源,能减少二氧化碳的排放,符合理念.
故选C.
点评 本题主要考查学生对绿色环保理念的理解及对常见污染的来源及治理等知识.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2. 屠呦呦因发现青蒿素荣(C15H22O5)获诺贝尔奖,青蒿素组成元素在元素周期表中的信息如图所示.下列说法不正确的是( )
屠呦呦因发现青蒿素荣(C15H22O5)获诺贝尔奖,青蒿素组成元素在元素周期表中的信息如图所示.下列说法不正确的是( )
 屠呦呦因发现青蒿素荣(C15H22O5)获诺贝尔奖,青蒿素组成元素在元素周期表中的信息如图所示.下列说法不正确的是( )
屠呦呦因发现青蒿素荣(C15H22O5)获诺贝尔奖,青蒿素组成元素在元素周期表中的信息如图所示.下列说法不正确的是( )| A. | 三种元素均属于非金属元素 | |
| B. | 氧离子(O2-)的核外电子数为8 | |
| C. | 三种元素的本质区别是核电荷数不同 | |
| D. | 质量相等的三种元素的原子,氢原子的个数最多 |
12.某校研究性学习小组在做“寻找新的催化剂”课题,研究思路是:氧化铜、氧化铁和二氧化锰均是金属氧化物,那么氧化铜、氧化铁是否也像二氧化锰一样可作过氧化氢或氯酸钾分解的催化剂,为此开展了以下探究,请你参与:
【探究一】验证二氧化锰能加快过氧化氢的分解
(1)请在如表的空白处填写相应的内容
(2)小组一部分同学依据实验①和②现象,就得出结论:二氧化锰能加快过氧化氢的分解.志强同学提出质疑,认为需增加一个对比实验③,才能得出结论,请你帮他填写如表空白:
(3)经过以上三个实验,可以得出结论:二氧化锰能加快过氧化氢的分解.请写出实验②的反应化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
【探究二】探究氧化铜、氧化铁是否像二氧化锰一样可作氯酸钾分解的催化剂按如表药品进行实验,用排水法收集氧气,当气泡连续均匀逸出时,测得数据如表(分解温度越低,催化效果越好):
(4)由实验⑥、⑦分别与实验④对比,可初步判断氧化铜、氧化铁也能作氯酸钾分解的催化剂.
(5)实验所用的三种金属氧化物中,催化效果最好的是二氧化锰.
(6)若要充分证明氧化铁是氯酸钾分解的催化剂,还要验证它在化学反应前后的质量和化学性质不变.请你设计实验验证其中一种“不变”:将实验⑦充分反应后的固体进行溶解、过滤、洗涤、干燥后称量,质量为1g,说明氧化铁在反应前后质量不变(写出实验步骤、现象和结论).
【探究一】验证二氧化锰能加快过氧化氢的分解
(1)请在如表的空白处填写相应的内容
| 实验编号 | 实验操作 | 实验现象 |
实验① | 取5%的过氧化氢溶液10 mL于试管中,过一会儿把带火星的木条伸入试管中 | 有少量气泡产生,木条不复燃 |
实验② | 取5%的过氧化氢溶液10mL于试管中,加入少量二氧化锰,把带火星的木条伸入试管中 | 有大量气泡产生,木条复燃 |
| 实验编号 | 实验操作 | 实验现象 |
实验③ | 取10mL蒸馏水于试管中,加入少量二氧化锰,把带火星的木条伸入试管中 | 无明显现象 |
【探究二】探究氧化铜、氧化铁是否像二氧化锰一样可作氯酸钾分解的催化剂按如表药品进行实验,用排水法收集氧气,当气泡连续均匀逸出时,测得数据如表(分解温度越低,催化效果越好):
| 实验编号 | 实验药品 | 分解温度(℃) |
| 实验④ | 1gKClO3 | 580 |
| 实验⑤ | 1gKClO3、1gMnO2 | 350 |
| 实验⑥ | 1gKClO3、1gCuO | 370 |
| 实验⑦ | 1gKClO3、1gFe2O3 | 390 |
(5)实验所用的三种金属氧化物中,催化效果最好的是二氧化锰.
(6)若要充分证明氧化铁是氯酸钾分解的催化剂,还要验证它在化学反应前后的质量和化学性质不变.请你设计实验验证其中一种“不变”:将实验⑦充分反应后的固体进行溶解、过滤、洗涤、干燥后称量,质量为1g,说明氧化铁在反应前后质量不变(写出实验步骤、现象和结论).
19.如图所示的实验操作中正确的是( )
| A. | 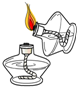 点燃酒精灯 | B. | 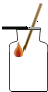 氧气验满 | C. | 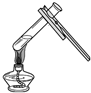 液体加热 | D. | 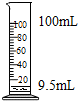 量9.5mL液体 |
17.下列有关NaOH的实验方案中,正确的是( )
| A. | 用NaOH固体干燥CO2气体 | |
| B. | 用酚酞溶液检验NaOH溶液是否变质 | |
| C. | 用熟石灰和纯碱为原料制取NaOH | |
| D. | 用CaCl2溶液除去NaOH溶液中的少量Na2CO3 |

 玻璃餐桌是当下时尚流行的元素,受到现代人的青睐,如图是一款玻璃餐桌的示意图.
玻璃餐桌是当下时尚流行的元素,受到现代人的青睐,如图是一款玻璃餐桌的示意图.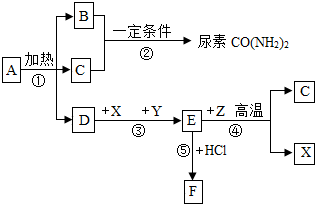 如图表示某些物质间转化关系.A为不含金属元素的盐,可作化肥,X是常见金属,B、C、Y、Z为气体,且B有刺激性气味,F为棕黄色溶液.
如图表示某些物质间转化关系.A为不含金属元素的盐,可作化肥,X是常见金属,B、C、Y、Z为气体,且B有刺激性气味,F为棕黄色溶液.