题目内容
14.如图是元素周期表的一部分,请回答相关问题: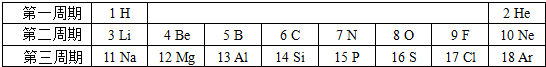
(1)氟元素与氯元素位于同一纵行的原因是原子核外电子层数相同.
(2)M2-与Ne核外电子排布相同,则M元素的名称为氧.
(3)写出1号、8号和11号三种元素组成化合物的化学式NaOH.
分析 (1)根据周期数=原子核外电子层数,进行分析解答.
(2)M2-与Ne核外电子排布相同,M2-是M原子得到2个电子得到的,进行分析解答.
(3)1号、8号和11号三种元素分别是氢元素、氧元素、钠元素,进行分析解答.
解答 解:(1)周期数=原子核外电子层数,氟元素与氯元素位于同一纵行的原因是原子核外电子层数相同.
(2)M2-与Ne核外电子排布相同,M2-是M原子得到2个电子得到的,其核外电子数为8;原子中质子数=核外电子数,则其核内质子数为8,为氧元素.
(3)1号、8号和11号三种元素分别是氢元素、氧元素、钠元素,其组成化合物的化学式为NaOH.
故答案为:(1)原子核外电子层数相同;(2)氧;(3)NaOH.
点评 本题难度不大,掌握周期数=原子核外电子层数、原子中质子数=核外电子数等是正确解答本题的关键.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
2. 如图是小徐用手掌总结氧气的化学性质的表示方法,手指上的物质能与手掌心氧气反应.则下列说法正确的是( )
如图是小徐用手掌总结氧气的化学性质的表示方法,手指上的物质能与手掌心氧气反应.则下列说法正确的是( )
 如图是小徐用手掌总结氧气的化学性质的表示方法,手指上的物质能与手掌心氧气反应.则下列说法正确的是( )
如图是小徐用手掌总结氧气的化学性质的表示方法,手指上的物质能与手掌心氧气反应.则下列说法正确的是( )| A. | 铁在空气中燃烧,生成四氧化三铁 | |
| B. | 煤脱硫的目的是减少二氧化硫的生成 | |
| C. | 磷燃烧产生大量的白雾,会污染空气 | |
| D. | 氧气的化学性质非常活泼,能与所有的物质反应 |
6.如图为某反应的微观示意图,下列有关说法正确的是( )

| A. | 该反应属于复分解反应 | |
| B. | A物质的化学式是NH3,其中氮元素的化合价为+3 | |
| C. | 该反应生成的氧化物的相对分子质量为18 | |
| D. | 化学反应前,原子和分子的总数都不变,但分子的种类一定改变 |
3.下列化学符号中的数字表示的意义不正确的是( )
| A. | 2Na:“2”表示两个钠元素 | |
| B. | 2OH-:“2”表示两个氢氧根离子 | |
| C. | $\stackrel{+2}{Mg}$:“+2”表示镁元素的化合价为+2 | |
| D. | NO2:“2”表示一个二氧化氮分子含有一个氧分子 |
4.药物“白炭灰”和“荻灰”在煎合过程中发生的反应属于( )
| A. | 氧化反应 | B. | 中和反应 | C. | 化合反应 | D. | 复分解反应 |
 在一次探究实验中,某学习小组将一定质量的高锰酸钾充分加热至不再放出气体为止,若试管中剩余固体的质量随时间变化关系如图所示.请计算:
在一次探究实验中,某学习小组将一定质量的高锰酸钾充分加热至不再放出气体为止,若试管中剩余固体的质量随时间变化关系如图所示.请计算: