题目内容
4.向某含有硫酸的100g废水样品中加入7.4g熟石灰,恰好完全反应(废水中的其它物质不参与反应).计算:该废水中含H2SO4的质量分数.分析 根据氢氧化钙和硫酸反应生成硫酸钙和水,结合氢氧化钙的质量计算反应的硫酸的质量,进一步计算该厂废水中硫酸的质量分数.
解答 解:设处理掉的硫酸质量为x
Ca(OH)2+H2SO4═CaSO4+2H2O
74 98
7.4g x
$\frac{74}{98}=\frac{7.4g}{x}$
x=9.8g
所以硫酸的质量分数为:$\frac{9.8g}{100g}$×100%=9.8%.
答:该废水中含H2SO4的质量分数为9.8%.
点评 本题主要考查学生运用化学方程式进行计算的能力,难度不大,题型基础.

练习册系列答案
相关题目
18.下列化学方程式书写完全正确的是( )
| A. | NaCl+KNO3═KCl+NaNO3 | B. | Fe2O3+3CO═2Fe+3CO2 | ||
| C. | Fe+2HCl═FeCl2+H2↑ | D. | 2Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 |
15.下列从实验现象中所得结论正确的是( )
| A. | 在某固体中滴加稀盐酸,有气泡产生,该固体一定是碳酸钙 | |
| B. | 某无色溶液中滴加硝酸银溶液,产生白色沉淀,则该溶液一定是稀盐酸 | |
| C. | 某无色溶液中滴加氯化钡溶液,产生白色沉淀,则该溶液一定是稀硫酸 | |
| D. | 某固态化肥与熟石灰混合研磨后产生氨臭味,该化肥一定是铵态氮肥 |
16.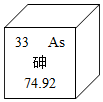 据新华网报道,英国某研究机构指出大米含致癌物质砷,专家建议4岁半以下儿童不应以米浆取代奶粉或人奶,以免摄取过量的砷.砷的部分信息如图,则说法正确的是( )
据新华网报道,英国某研究机构指出大米含致癌物质砷,专家建议4岁半以下儿童不应以米浆取代奶粉或人奶,以免摄取过量的砷.砷的部分信息如图,则说法正确的是( )
 据新华网报道,英国某研究机构指出大米含致癌物质砷,专家建议4岁半以下儿童不应以米浆取代奶粉或人奶,以免摄取过量的砷.砷的部分信息如图,则说法正确的是( )
据新华网报道,英国某研究机构指出大米含致癌物质砷,专家建议4岁半以下儿童不应以米浆取代奶粉或人奶,以免摄取过量的砷.砷的部分信息如图,则说法正确的是( )| A. | 砷属于金属元素 | B. | 砷原子的最外层电子数是33 | ||
| C. | 砷原子的质子数是33 | D. | 砷的相对原子质量是74.92 |
 书包是学生必备的日常工具,其制作材料有①尼龙面料②塑料把手③金属拉链等.
书包是学生必备的日常工具,其制作材料有①尼龙面料②塑料把手③金属拉链等.
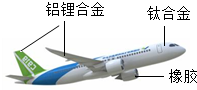 (1)图中标示的材料中,属于有机合成材料的是橡胶;
(1)图中标示的材料中,属于有机合成材料的是橡胶;