题目内容
 酸、碱、盐、氧化物是初中化学中重要的物质,利用各物质的性质都可以制取盐,根据图中关系回答下列问题:
酸、碱、盐、氧化物是初中化学中重要的物质,利用各物质的性质都可以制取盐,根据图中关系回答下列问题:(1)写出能与稀盐酸反应的一种金属
(2)写出一种碱与盐反应的方程式
(3)利用硝酸钠和硫酸钾制取硝酸钾,能否达到目的?
(4)氢氧化钠溶液在空气中易变质是因为碱易与
考点:物质的相互转化和制备,酸的化学性质,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:(1)排在氢前边的金属都能与盐酸反应产生氢气;(2)碱与盐反应生成新碱和新盐,反应物中的碱和盐必须溶于水;(3)根据复分解反应发生的条件考虑;(4)氢氧化钠变质时由于氢氧化钠与二氧化碳反应生成碳酸钠和水.
解答:解:(1)排在氢前边的金属都能与盐酸反应产生氢气,所以铁能与盐酸反应生成氯化亚铁和氢气;
(2)氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,用观察法配平即可,所以方程式是:Ca(OH)2+Na2CO3═2NaOH+CaCO3↓;
(3)复分解反应发生的条件:生成物中有沉淀生成、或水生成、或气体放出,硝酸钠与硫酸钾反应,既不能产生气体、沉淀也不能产生水,不符合复分解反应的条件,不能发生反应;
(4)氢氧化钠与二氧化碳反应生成碳酸钠而变质.
故答案为:(1)铁;(2)Ca(OH)2+Na2CO3═2NaOH+CaCO3↓;(3)不能;反应后没有沉淀、气体或水生成;(4)CO2(或二氧化碳).
(2)氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,用观察法配平即可,所以方程式是:Ca(OH)2+Na2CO3═2NaOH+CaCO3↓;
(3)复分解反应发生的条件:生成物中有沉淀生成、或水生成、或气体放出,硝酸钠与硫酸钾反应,既不能产生气体、沉淀也不能产生水,不符合复分解反应的条件,不能发生反应;
(4)氢氧化钠与二氧化碳反应生成碳酸钠而变质.
故答案为:(1)铁;(2)Ca(OH)2+Na2CO3═2NaOH+CaCO3↓;(3)不能;反应后没有沉淀、气体或水生成;(4)CO2(或二氧化碳).
点评:解答本题关键是要知道金属与酸反应的条件,复分解反应发生的条件,氢氧化钠容易变质的原因.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图是密闭系统中发生的反应的微观示意图,其中“○”和“●”分别表示两种不同的原子A和B.下列说法正确的是( )


| A、该反应可表示为2AB+2B2═2AB2+B2 |
| B、该反应属于置换反应 |
| C、反应物中的化合物可能是氧化物 |
| D、在化学反应中,分子的大小、质量和数目都不变 |
某同学想用实验证明CuSO4溶液显蓝色是由Cu2+造成的,下列实验无意义的是( )
| A、将CuSO4溶液加水稀释 |
| B、观察Cu(NO3)2溶液的颜色 |
| C、观察Na2SO4溶液的颜色 |
| D、向CuSO4溶液中滴加足量NaOH溶液观察溶液的颜色 |
 某化学兴趣小组利用所学知识测定锌铜合金中铜的质量分数.
某化学兴趣小组利用所学知识测定锌铜合金中铜的质量分数.
 如图表示某些物质间转化关系(反应条件和部分产物已省略).其中A、E为固体氧化物,且A为黑色粉末;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是最常见的金属.
如图表示某些物质间转化关系(反应条件和部分产物已省略).其中A、E为固体氧化物,且A为黑色粉末;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是最常见的金属.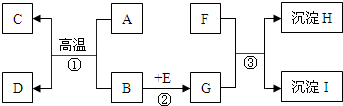
 早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁反应.某化学兴趣小组利用图装置进行实验探究.
早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁反应.某化学兴趣小组利用图装置进行实验探究.