题目内容
4.根据如图所示的实验装置,回答问题:
氨气(NH3)是一种无色有刺激性气味,极易溶于水的气体.实验室常用氯化铵晶体和氢氧化钙粉末混合加热来制取氨气同时还生成氯化钙和水.写出制取氨气的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;选取上述A(填字母)作为制取氨气的发生装置;收集氨气只能选用的装置为D(填字母),其原因是氨气的密度比空气小,不能用C装置收集,氨气易溶于水,不能用E装置收集,因此只能够用D装置收集.
分析 根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置.
解答 解:氯化铵晶体和氢氧化钙粉末在加热条件下反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
因为反应需要加热,应该用A装置作为发生装置;
氨气极易溶于水,不能用排水法收集,即不能用E装置收集,密度比空气小,可以用向下排空气法收集,即用D装置收集,不能用C装置收集.
故填:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;A;D;氨气的密度比空气小,不能用C装置收集,氨气易溶于水,不能用E装置收集,因此只能够用D装置收集.
点评 本题主要考查反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

练习册系列答案
相关题目
14.在日常生活中,下列做法正确的是( )
| A. | 用甲醛溶液浸泡海参 | |
| B. | 用霉变的谷物当鸡鸭饲料 | |
| C. | 焙制糕点时加入小苏打 | |
| D. | 为了防止甲状腺病,长期摄入过量的碘元素 |
15.阿莫西林是一种常见的抗生素,其化学式为C16H19N3O5S,下列说法正确的是( )
| A. | 阿莫西林中含有16个碳原子 | |
| B. | 阿莫西林是由五种元素组成的 | |
| C. | 阿莫西林中氢、氮元素质量比为19:3 | |
| D. | 阿莫西林中氮元素的质量分数为16.7% |
12.下列区分物质的方法不正确的是( )
| A. | 用肥皂水区分硬水和软水 | |
| B. | 用水区分硝酸铵固体和氢氧化钠固体 | |
| C. | 用稀盐酸检验氢氧化钠是否变质 | |
| D. | 用酚酞溶液区分稀盐酸和食盐水 |
16.0.80g CuSO4•5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示.下列说法正确的是( )


| A. | 200℃时固体物质的化学式为CuSO4•H2O | |
| B. | CuSO4•5H2O在110℃时可以稳定存在 | |
| C. | CuSO4•5H2O失去结晶水的过程是一个物理变化 | |
| D. | 将2.5gCuSO4•5H2O溶于7.5g水中,所得溶液的质量分数为25% |
14.下列图象能正确反映对应变化关系的是( )
| A. |  向铜、锌混合物粉末中加入盐酸 | |
| B. | 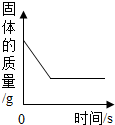 将铜片加入到一定量的硝酸银溶液中 | |
| C. | 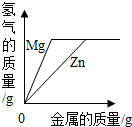 向两份完全相同的稀盐酸中分别加入锌粉、镁粉 | |
| D. |  向两份完全相同的稀盐酸中分别加入锌粉、镁粉 |
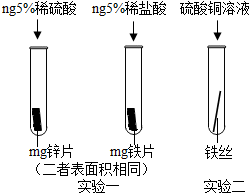 铁元素与人类的关系密切.
铁元素与人类的关系密切.