题目内容
14.在实验室里,可以利用图1装置制得铁.(1)A处玻璃管内所发生反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)C处酒精灯的作用是处理尾气.
(3)待红色的氧化铁完全变黑后,在A处停止加热,是否不需要(填“需要”或“不需要”)断开装置A、B的连接处以防B中石灰水倒吸入A中.理由是需要继续通入一氧化碳直到玻璃管冷却.
(4)玻璃管中的黑色粉末全部是铁粉吗?小华对此进行了初步探究(见图2):

①请写出铁粉与硫酸铜溶液反应的化学方程式Fe+CuSO4=FeSO4+Cu.实验过程中采取了过滤,该操作中用到的玻璃仪器有烧杯、漏斗和玻璃棒,其中玻璃棒的作用是引流.
②根据小华的实验结果你认为玻璃管中的黑色粉末不全部(填“全部”或“不全部”)是铁粉,理由是得到的固体中含有黑色粉末.
分析 (1)根据在高温条件下一氧化碳与氧化铁的反应写出反应的化学方程式;
(2)根据尾气中含有有毒的一氧化碳来分析解答;
(3)根据实验的步骤和注意事项分析回答;
(4)根据铁与硫酸铜的反应和过滤的操作分析回答.
解答 解:(1)A处玻璃管内所发生反应是一氧化碳和氧化铁在高温条件下反应生成了铁和二氧化碳,方程式是:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)CO有毒,排放到空气中会污染大气,应对尾气进行处理,.所以C处酒精灯的作用是处理尾气.
(3)待红色的氧化铁完全变黑后,在A处停止加热,不需要断开装置A、B的连接处以防B中石灰水倒吸入A中.理由是需要继续通入一氧化碳直到玻璃管冷却.
(4)①铁粉与硫酸铜溶液反应生成了铜和硫酸亚铁,反应的化学方程式是:Fe+CuSO4=FeSO4+Cu.实验过程中采取了过滤,该操作中用到的玻璃仪器有烧杯、漏斗和玻璃棒,其中玻璃棒的作用是引流.
②由于硫酸铜是足量的,能将铁完全反应,根据小华的实验结果可知,玻璃管中的黑色粉末不全部是铁粉,理由是得到的固体中含有黑色粉末.
故答案为:(1)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)处理尾气;
(3)不需要,需要继续通入一氧化碳直到玻璃管冷却.
(4)①Fe+CuSO4=FeSO4+Cu,烧杯,漏斗,引流.②不全部,得到的固体中含有黑色粉末.
点评 本题是通过实验装置图考查了一氧化碳还原氧化铁的实验,要求学生必须动手做实验的同时,学会观察实验,分析实验.知道一氧化碳还原氧化铁的注意事项,尾气的处理方法.

练习册系列答案
相关题目
5.河水净化的主要步骤如图所示,有关说法错误的是( )
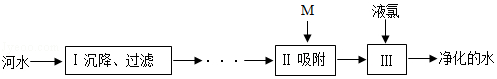

| A. | 步骤I可除去难溶性杂质 | |
| B. | 加试剂M是为了除去有颜色、气味的物质 | |
| C. | 净水的过程都属于属于物理变化 | |
| D. | 净化后的水仍是混合物 |
3.下列化学用语与含义相符的是( )
| A. | O2-两个氧原子 | B. | 3H-3个氢元素 | ||
| C. | Fe3O4-四氧化三铁 | D. | Ca+2-钙离子 |
4.环境、能源和资源是人类生存和发展的基本条件,下列说法不正确的是( )
| A. | 空气是一种宝贵的自然资源,其中含量最高的氮气体积分数约为78% | |
| B. | 目前已经广泛用塑料来代替钢和其他合金制造管道、齿轮和汽车零件等 | |
| C. | 地壳中含有最多的金属元素是铝,人类每年在自然界中提取最多的金属是铁 | |
| D. | 海洋是最大的资源宝库,其中含有80多种金属元素 |
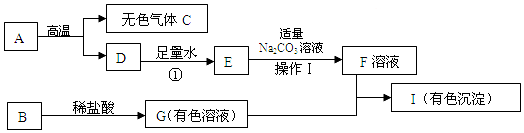
 A~F都是初中化学中的常见物质,且有如图所示转化关系(反应条件、部分生成物均已略去).
A~F都是初中化学中的常见物质,且有如图所示转化关系(反应条件、部分生成物均已略去).