题目内容
12.用化学用语填空(1)氖气:Ne
(2)2个镁离子:2Mg2+
(3)标出相对分子质量最小的氧化物中氧元素的化合价:H2$\stackrel{-2}{O}$
(4)高锰酸钾中所含的阴离子:Mn${{O}_{4}}^{-}$.
分析 (1)根据氖气是单原子分子进行分析;
(2)根据离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字进行分析;
(3)根据相对分子质量最小的氧化物是水进行分析;
(4)根据高锰酸钾中所含的阴离子是高锰酸根离子进行分析.
解答 解:(1)氖气是单原子分子,化学式为:Ne;
(2)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,所以2个镁离子表示为:2Mg2+;
(3)相对分子质量最小的氧化物是水,所以水氧元素的化合价表示为:H2$\stackrel{-2}{O}$;
(4)高锰酸钾中所含的阴离子是高锰酸根离子,表示为:Mn${{O}_{4}}^{-}$.
故答案为:(1)Ne;
(2)2Mg2+;
(3)H2$\stackrel{-2}{O}$;
(4)Mn${{O}_{4}}^{-}$.
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
17.如图所示的操作中,不正确的是( )
| A. | 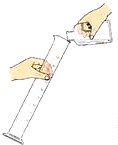 | B. | 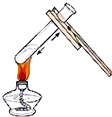 | C. | 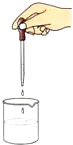 | D. | 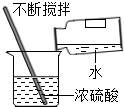 |
4.研究金属的腐蚀对资源的利用和保护意义重大.
(1)为了探究铁锈蚀的条件,进行如图所示实验.经过一周后观察,试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.
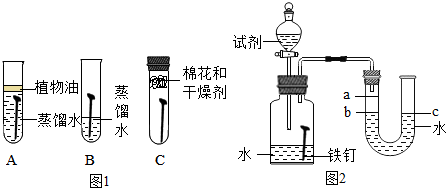
①通过实验发现:铁锈蚀是铁与氧气和水发生化学反应的过程.
②A中加入的蒸馏水要事先煮沸,其目的是除去水中的氧气.
(2)家中的刀具若沾有食盐水锈蚀更快.为了进一步探究影响铁锈蚀速率的因素,做了如下的实验.
【提出问题】铁锈蚀速率与哪些因素有关.
【查阅资料】①物质溶解在水中得到的混合物称为水溶液,如氯化钠溶解在水中得到氯化钠溶液,乙醇溶解在水中得到乙醇溶液.
②氯化钠溶液能导电;乙醇溶液不能导电.
【猜想】铁的锈蚀速率与下列因素有关:
①反应时的温度;②水溶液的导电性.
【实验】每次取两套如图所示的装置,编号为I、II.向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致).
(1)为了探究铁锈蚀的条件,进行如图所示实验.经过一周后观察,试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.

①通过实验发现:铁锈蚀是铁与氧气和水发生化学反应的过程.
②A中加入的蒸馏水要事先煮沸,其目的是除去水中的氧气.
(2)家中的刀具若沾有食盐水锈蚀更快.为了进一步探究影响铁锈蚀速率的因素,做了如下的实验.
【提出问题】铁锈蚀速率与哪些因素有关.
【查阅资料】①物质溶解在水中得到的混合物称为水溶液,如氯化钠溶解在水中得到氯化钠溶液,乙醇溶解在水中得到乙醇溶液.
②氯化钠溶液能导电;乙醇溶液不能导电.
【猜想】铁的锈蚀速率与下列因素有关:
①反应时的温度;②水溶液的导电性.
【实验】每次取两套如图所示的装置,编号为I、II.向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致).
| 影响因素 | 实验设计实验 | 现象 | 实验结论 |
| ①温度 | 装置I放入25℃恒温环境中,装置II放入40℃恒温环境中. | 两套装置中铁钉均锈蚀,且U型管中液面均由b处上升至a处,则所需时间I>II. | 铁的锈蚀速率与反应时的温度有关, 温度越高,铁的锈蚀速率越快 |
| ②水溶液的导电性 | 在相同温度下,装置I集气瓶中加入10mL氯化钠溶液;装置II集气瓶中加入10mL乙醇. | 两套装置中铁钉均锈蚀;且U型管中液面均由b处上升至a处,则所需时间I<II. | 铁的锈蚀速率与水溶液的导电性有关,在能导电的溶液中,锈蚀的速率加快 |
 ;
; A-G为中学化学常见物质,其中C、E、G为无色气体,F为红色金属,反应③是炼铁工业中的主要反应,它们之间的相互转化关系如图所示:
A-G为中学化学常见物质,其中C、E、G为无色气体,F为红色金属,反应③是炼铁工业中的主要反应,它们之间的相互转化关系如图所示: