题目内容
甲、乙、丙三位同学在活动课上探究气体的制备,利用如图1所示装置制取常见的气体,并对它们的有关性质进行研究,请根据题意回答下列问题.
(1)甲同学用一种盐类固体制取O2,发生和收集装置应选用图1中的 装置(填编号),该反应的化学方程式为 ;当用装置C收集满并取出集气瓶后,停止该实验的正确操作方法是 .
(2)乙同学用浓盐酸与大理石在F装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,对这一现象的解释合理是 (填序号).
a.产生的CO2直接使石蕊变红
b.产生的CO2与H2O反应生成H2CO3,使石蕊试液变红
c.挥发出的氯化氢溶于水,使石蕊试液变红
(3)丙同学在实验室氯化铵固体与碱石灰固体共热来制取氨气(NH3).常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.则制取并收集NH3,应该从图中选择的制取装置是 .NH3是一种碱性气体,干燥时不能选用下列干燥剂中的 .(填序号).
A.固体氢氧化钠 B.浓硫酸 C.生石灰
(4)在实验室中,集气瓶被称为“万能瓶”,用它可以组装成各种用途的装置,请仔细观察图2下列(F-K)各个装置的特点回答问题:
①实验室若用F装置收集氧气,则氧气应从 口进入(填导管口符号)
②若要收集一定体积的二氧化碳气体,应选用 装置.
③若要除去一氧化碳中的少量二氧化碳,同时用该瓶收集较纯净的一氧化碳,应选用 装置.

(1)甲同学用一种盐类固体制取O2,发生和收集装置应选用图1中的
(2)乙同学用浓盐酸与大理石在F装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,对这一现象的解释合理是
a.产生的CO2直接使石蕊变红
b.产生的CO2与H2O反应生成H2CO3,使石蕊试液变红
c.挥发出的氯化氢溶于水,使石蕊试液变红
(3)丙同学在实验室氯化铵固体与碱石灰固体共热来制取氨气(NH3).常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.则制取并收集NH3,应该从图中选择的制取装置是
A.固体氢氧化钠 B.浓硫酸 C.生石灰
(4)在实验室中,集气瓶被称为“万能瓶”,用它可以组装成各种用途的装置,请仔细观察图2下列(F-K)各个装置的特点回答问题:
①实验室若用F装置收集氧气,则氧气应从
②若要收集一定体积的二氧化碳气体,应选用
③若要除去一氧化碳中的少量二氧化碳,同时用该瓶收集较纯净的一氧化碳,应选用
考点:常用气体的发生装置和收集装置与选取方法,分离物质的仪器,实验室制取氧气的反应原理,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)甲同学用一种盐类固体制取O2,这种盐可以选取高锰酸钾;利用高锰酸钾制氧气是固体加热;氧气密度比空气大,且不易溶于水,依此可选择合适的发生和收集装置;本题用排水法收集气体时,为防止水槽里的水倒吸入试管里,停止该实验的正确操作方法应该是先把导气管移出水面,然后撤去酒精灯.
(2)用浓盐酸与大理石在F装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,说明烧杯中的液体显酸性,分析造成这种结果的原因即可解答;
(3)加热氯化铵和氢氧化钙的固体混合物制取氨气,氨气极易溶于水,这就决定了制取氨气必须在干燥的环境下;NH3是一种碱性气体,干燥时不能选用酸性的干燥剂;
(4)①因为氧气的密度比空气的大,所以氧气从b口进入.
②要收集一定体积的二氧化碳气体,选用量筒,且二氧化碳可溶于水,所以用植物油起隔离作用;
③若要除去一氧化碳中的少量二氧化碳,可以与石灰水或水反应,且一氧化碳不与石灰水或水反应据此作答.
(2)用浓盐酸与大理石在F装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,说明烧杯中的液体显酸性,分析造成这种结果的原因即可解答;
(3)加热氯化铵和氢氧化钙的固体混合物制取氨气,氨气极易溶于水,这就决定了制取氨气必须在干燥的环境下;NH3是一种碱性气体,干燥时不能选用酸性的干燥剂;
(4)①因为氧气的密度比空气的大,所以氧气从b口进入.
②要收集一定体积的二氧化碳气体,选用量筒,且二氧化碳可溶于水,所以用植物油起隔离作用;
③若要除去一氧化碳中的少量二氧化碳,可以与石灰水或水反应,且一氧化碳不与石灰水或水反应据此作答.
解答:解:
(1)甲同学用一种盐类固体制取O2,这种盐可以选取高锰酸钾;利用高锰酸钾制氧气是固体加热,装置是A;
因为氧气密度比空气大,且不易溶于水,所以收集装置可以是C;
该反应的化学方程式为:2KMnO4
K2MnO4+MnO2+2O2↑;
当用装置C收集满并取出集气瓶后,为防止水槽里的水倒吸入试管里,停止该实验的正确操作方法应该是先把导气管移出水面,然后撤去酒精灯.
(2)乙同学用浓盐酸与大理石在F装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,说明烧杯中的液体显酸性,这种结果是有两个方面的原因造成的:一是产生的CO2与H2O反应生成H2CO3,二是挥发出的氯化氢溶于水,所以对这一现象的解释合理选项是:bc;
(3)加热氯化铵和氢氧化钙的固体混合物制取氨气,氨气极易溶于水,这就决定了制取氨气必须在干燥的环境下,所以应该从图中选择的制取装置是A;NH3是一种碱性气体,干燥时不能选用酸性的干燥剂,干燥时不能选用所列干燥剂中的B;
(4)①因为氧气的密度比空气的大,所以氧气从b口进入.
②要收集一定体积的二氧化碳气体,选用量筒,且二氧化碳可溶于水,所以用植物油起隔离作用,故选用K装置.
③若要除去一氧化碳中的少量二氧化碳,可以与石灰水或水反应,且一氧化碳不与石灰水或水反应,所以若要除去一氧化碳中的少量二氧化碳,同时用该瓶收集较纯净的一氧化碳,因为G装置中存有部分空气,故应选用H装置.
故答案为:
(1)AC;2KMnO4
K2MnO4+MnO2+2O2↑;先把导气管移出水面,然后撤去酒精灯;
(2)bc;
(3)A;B;
(4)①b;②K;③H.
(1)甲同学用一种盐类固体制取O2,这种盐可以选取高锰酸钾;利用高锰酸钾制氧气是固体加热,装置是A;
因为氧气密度比空气大,且不易溶于水,所以收集装置可以是C;
该反应的化学方程式为:2KMnO4
| ||
当用装置C收集满并取出集气瓶后,为防止水槽里的水倒吸入试管里,停止该实验的正确操作方法应该是先把导气管移出水面,然后撤去酒精灯.
(2)乙同学用浓盐酸与大理石在F装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,说明烧杯中的液体显酸性,这种结果是有两个方面的原因造成的:一是产生的CO2与H2O反应生成H2CO3,二是挥发出的氯化氢溶于水,所以对这一现象的解释合理选项是:bc;
(3)加热氯化铵和氢氧化钙的固体混合物制取氨气,氨气极易溶于水,这就决定了制取氨气必须在干燥的环境下,所以应该从图中选择的制取装置是A;NH3是一种碱性气体,干燥时不能选用酸性的干燥剂,干燥时不能选用所列干燥剂中的B;
(4)①因为氧气的密度比空气的大,所以氧气从b口进入.
②要收集一定体积的二氧化碳气体,选用量筒,且二氧化碳可溶于水,所以用植物油起隔离作用,故选用K装置.
③若要除去一氧化碳中的少量二氧化碳,可以与石灰水或水反应,且一氧化碳不与石灰水或水反应,所以若要除去一氧化碳中的少量二氧化碳,同时用该瓶收集较纯净的一氧化碳,因为G装置中存有部分空气,故应选用H装置.
故答案为:
(1)AC;2KMnO4
| ||
(2)bc;
(3)A;B;
(4)①b;②K;③H.
点评:本题考查内容较多,多属于基础性问题,只要知识熟练,细心作答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
法国化学家肖万、美国化学家格拉布斯和施罗克在有机化学领域研究中作出了重要贡献,其研究成果可以简单描述为如下的反应(R1~R8为H-、CH3-、C2H5-…等).
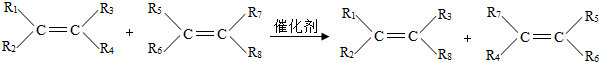
上述反应类似于无机反应中的( )

上述反应类似于无机反应中的( )
| A、置换反应 | B、分解反应 |
| C、化合反应 | D、复分解反应 |


 已知A、B、C、D、E是初中化学常见的物质,D物质的水溶液为蓝色,E是相对分子质量最小的氧化物,它们的转化关系如图所示:
已知A、B、C、D、E是初中化学常见的物质,D物质的水溶液为蓝色,E是相对分子质量最小的氧化物,它们的转化关系如图所示: 如图是某胃药标签上的部分内容,某中学化学兴趣小组欲测定该药品中碳酸氢钠(NaHCO3)的质量分数,取10片该药品研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(杂质不溶于水,也不参加反应.反应的化学方程式为
如图是某胃药标签上的部分内容,某中学化学兴趣小组欲测定该药品中碳酸氢钠(NaHCO3)的质量分数,取10片该药品研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(杂质不溶于水,也不参加反应.反应的化学方程式为