题目内容
海边盛产贝壳,其主要成分为CaCO3,以贝壳和纯碱为原料,生产烧碱的简要工艺流程如图:
请回答下列问题:
(1)A的化学式是 .
(2)写出步骤③发生反应的化学方程式 .
(3)在工业上,熟石灰可用于生产烧碱.在农业上,它的一种用途是: .

请回答下列问题:
(1)A的化学式是
(2)写出步骤③发生反应的化学方程式
(3)在工业上,熟石灰可用于生产烧碱.在农业上,它的一种用途是:
考点:碳酸钙、生石灰、熟石灰之间的转化,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:碳酸钙分解生成氧化钙,熟石灰--氢氧化钙和纯碱--碳酸钠反应生成碳酸钙沉淀和氢氧化钠,据反应原理书写方程式;并结合氢氧化钙的用途分析解答.
解答:解:(1)贝壳,其主要成分为CaCO3,碳酸钙在高温下生成氧化钙和二氧化碳,所以A为氧化钙,化学式为CaO;
(2)熟石灰--氢氧化钙能与纯碱--碳酸钠反应生成氢氧化钠和碳酸钙沉淀,反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(3)在工业上,熟石灰可用于生产烧碱.在农业上,熟石灰可用来改良酸性土壤.
故答案为:(1)CaO;
(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(3)改良酸性土壤.
(2)熟石灰--氢氧化钙能与纯碱--碳酸钠反应生成氢氧化钠和碳酸钙沉淀,反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(3)在工业上,熟石灰可用于生产烧碱.在农业上,熟石灰可用来改良酸性土壤.
故答案为:(1)CaO;
(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(3)改良酸性土壤.
点评:掌握碳酸钙、氧化钙、氢氧化钙之间的转化关系、物质的用途等是正确解答本题的关键.

练习册系列答案
相关题目
“化学伴我身边,变化无处不在”,以下变化属于化学变化的是( )
| A、榨取果汁 | B、点燃煤气 |
| C、白酒挥发 | D、食盐溶解 |
下列现象一定能说明物质发生化学变化的是( )
| A、发光放热 | B、燃烧 |
| C、爆炸 | D、变色 |
一包白色粉末,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成,为探究其组成,进行如下实验:
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;
(2)取实验(1)滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体
则下列有关说法正确的是( )
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;
(2)取实验(1)滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体
则下列有关说法正确的是( )
| A、该白色粉末的成分中一定不含有CuSO4 |
| B、该白色粉末的成分中一定不含有NaOH |
| C、该白色粉末的组成有5种可能 |
| D、若向实验(1)得到的滤液中,通入二氧化碳,产生白色沉淀,则可推断原白色粉末由CaCO3和BaCl2组成 |
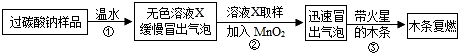
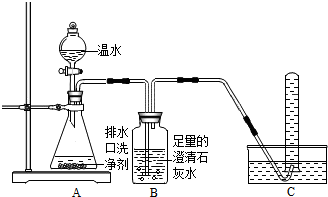 小明同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.
小明同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.