题目内容
 卫生部等7部委联合发布公告,禁止在面粉生产中添加过氧化钙(用作面粉增白).李明同学闻知后,对过氧化钙很感兴趣,就去买了一些回来做实验.
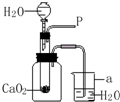
卫生部等7部委联合发布公告,禁止在面粉生产中添加过氧化钙(用作面粉增白).李明同学闻知后,对过氧化钙很感兴趣,就去买了一些回来做实验.(1)李明使用如图所示的装置进行实验,打开分液漏斗的活塞,控制滴加水的速度,观察到试管内缓缓产生少量气泡,用带火星的木条靠近P处,木条复燃,说明生成的气体是
(2)根据质量守恒定律,李明认为过氧化钙与过量水反应还应产生某种含钙元素的物质.开始李明假设该产物为CaO,但通过思考他很快否定了原先的假设,并重新假设生成的含钙产物为Ca(OH)2.请解释李明否定原假设建立新假设的理由
(3)李明通过实验证明了过氧化钙与水反应的确有氢氧化钙生成,请写出过氧化钙和水反应的化学方程式
(4)李明在实验时观察到烧杯中有气泡产生,由此他还得出的结论是
(5)李明同学查阅资料后发现,许多养鱼的人会在活鱼的运输过程中往水中加入少量过氧化钙,他认为这么做的目的是
考点:实验探究物质的性质或变化规律,氧气的检验和验满,生石灰的性质与用途,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据氧气的检验方法进行分析解答;
(2)根据氧化钙的性质来分析过氧化钙与水反应的产物;
(3)根据质量守恒定律,过氧化钙它与水反应生成氧气和氢氧化钙,写出反应的化学方程式即可;
(4)因瓶中装置内有空气,利用烧杯a中有气泡产生来说明反应是否放热.
(5)根据鱼的生存需要氧气来分析相鱼塘中加入过氧化钙的目的;
(2)根据氧化钙的性质来分析过氧化钙与水反应的产物;
(3)根据质量守恒定律,过氧化钙它与水反应生成氧气和氢氧化钙,写出反应的化学方程式即可;
(4)因瓶中装置内有空气,利用烧杯a中有气泡产生来说明反应是否放热.
(5)根据鱼的生存需要氧气来分析相鱼塘中加入过氧化钙的目的;
解答:解:(1)氧气能使带火星的木条复燃,用带火星木条进行实验,发现木条复燃,则释放出来的是氧气,故答案为:氧气;
(2)因氧化钙能与水发生化学反应,则在水中不会生成氧化钙,则可能生成氢氧化钙,故答案为:在水中因氧化钙会与水化合生成Ca(OH)2;
(3)根据质量守恒定律,过氧化钙与水反应生成使带火星的木条复燃的氧气和显碱性的氢氧化钙,用奇偶法配平,反应的化学方程式为2CaO2+2H2O═2Ca(OH)2+O2↑,故答案为:2CaO2+2H2O═2Ca(OH)2+O2↑;
(4)因由烧杯a中有气泡产生,则可知装置中的瓶子内空气受热膨胀导致的,所以可判断反应放热,故答案为:CaO2与水的反应为放热反应;
(5)养鱼的农民有时向鱼塘中撒过氧化钙是为了得到较多的氧气来供鱼类呼吸,故答案为:给鱼供氧.
(2)因氧化钙能与水发生化学反应,则在水中不会生成氧化钙,则可能生成氢氧化钙,故答案为:在水中因氧化钙会与水化合生成Ca(OH)2;
(3)根据质量守恒定律,过氧化钙与水反应生成使带火星的木条复燃的氧气和显碱性的氢氧化钙,用奇偶法配平,反应的化学方程式为2CaO2+2H2O═2Ca(OH)2+O2↑,故答案为:2CaO2+2H2O═2Ca(OH)2+O2↑;
(4)因由烧杯a中有气泡产生,则可知装置中的瓶子内空气受热膨胀导致的,所以可判断反应放热,故答案为:CaO2与水的反应为放热反应;
(5)养鱼的农民有时向鱼塘中撒过氧化钙是为了得到较多的氧气来供鱼类呼吸,故答案为:给鱼供氧.
点评:本题难度不大,考查同学们灵活运用所学氧气的检验、化学方程式的书写等知识进行解题的能力

练习册系列答案
相关题目
对于化学反应A+B═C+D.的下列说法中,正确的是( )
| A、若A和D都是氧化物,则B和C中有可能再有氧化物 |
| B、若C和D分别是盐和水,则该反应一定是中和反应 |
| C、若A是可溶性碱,B是可溶性盐,则C和D不可能都是沉淀 |
| D、若A和C都是单质,B和D都是化合物,则该反应一定是置换反应 |
 化学是以实验为基础的自然科学,如图所示为实验室常用的实验装置.
化学是以实验为基础的自然科学,如图所示为实验室常用的实验装置.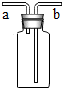 如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题
如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题