题目内容
科学家经过多年研究证明,某些零食中含一定量的有害物质,如油炸食品中常含有致癌物质丙烯酰胺(C3H5NO).
(1)丙烯酰胺的相对分子质量是 .
(2)丙烯酰胺中碳元素和氧元素的质量比是 .
(3)建议:每天丙烯酰胺的摄入量(按体重计)不多于1 μg/kg.60g珍珍牌薯片中含丙烯酰胺150 μg.若你的体重为50kg,你每天最多吃这种薯片 g.
(1)丙烯酰胺的相对分子质量是
(2)丙烯酰胺中碳元素和氧元素的质量比是
(3)建议:每天丙烯酰胺的摄入量(按体重计)不多于1 μg/kg.60g珍珍牌薯片中含丙烯酰胺150 μg.若你的体重为50kg,你每天最多吃这种薯片
考点:相对分子质量的概念及其计算,元素质量比的计算
专题:化学式的计算
分析:(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据题意,每天丙烯酰胺的摄入量(按体重计)不多于1 μg/kg.60g珍珍牌薯片中含丙烯酰胺150 μg;据此计算体重为50kg每天最多吃这种薯片的质量即可.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据题意,每天丙烯酰胺的摄入量(按体重计)不多于1 μg/kg.60g珍珍牌薯片中含丙烯酰胺150 μg;据此计算体重为50kg每天最多吃这种薯片的质量即可.
解答:解:(1)丙烯酰胺的相对分子质量是12×3+1×5+16+14=71.
(2)丙烯酰胺中碳元素和氧元素的质量比是(12×3):16=9:4.
(3)每天丙烯酰胺的摄入量(按体重计)不多于1 μg/kg,则体重为50kg,每天丙烯酰胺的摄入量为1 μg/kg×50kg=50μg;60g珍珍牌薯片中含丙烯酰胺,则每天最多吃这种薯片的质量为60g×
=20g.
故答案为:(1)71;(2)9:4;(3)20.
(2)丙烯酰胺中碳元素和氧元素的质量比是(12×3):16=9:4.
(3)每天丙烯酰胺的摄入量(按体重计)不多于1 μg/kg,则体重为50kg,每天丙烯酰胺的摄入量为1 μg/kg×50kg=50μg;60g珍珍牌薯片中含丙烯酰胺,则每天最多吃这种薯片的质量为60g×
| 50μg |
| 150μg |
故答案为:(1)71;(2)9:4;(3)20.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
下列说法中正确的是( )
| A、化学反应常常伴随有能量变化,因此有能量变化的都是化学变化 |
| B、金刚石和C60的组成元素相同,原子排列方式不同,因此它们的物理性质存在差异 |
| C、某白色固体与熟石灰研磨,产生的气体可使酚酞溶液变成红色,则该固体是铵盐 |
| D、等质量的Na2CO3和NaHCO3分别与足量盐酸反应产生等质量的CO2 |
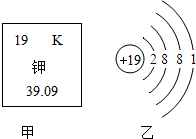 钾在自然界没有单质形态存在,钾元素以盐的形式广泛分布于陆地和海洋中,钾也是人体肌肉组织和神经组织中的重要成分之一.根据图2所示的相关信息判断,下列说法正确的是( )
钾在自然界没有单质形态存在,钾元素以盐的形式广泛分布于陆地和海洋中,钾也是人体肌肉组织和神经组织中的重要成分之一.根据图2所示的相关信息判断,下列说法正确的是( )| A、其相对原子质量为19 |
| B、图2-甲中元素符号写错,应该为K |
| C、钾原子中有19个中子 |
D、其离子结构为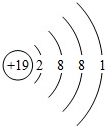 |
日本福岛第一核电站发生严重的核辐射泄漏,已知核辐射中放射性碘(碘-131)的核电荷数为53,(元素符号I)则下列说法正确的是( )
| A、已知碘元素的原子与氯元素的原子最外层电子均是7,则碘化钠的化学式为Na2I |
| B、科学食用加碘食盐可以预防甲状腺疾病 |
| C、碘I-127原子和放射性碘原子I-131原子的中子数不同,不属于同种元素 |
| D、碘几乎不溶于水,却可以溶于汽油中,说明在相同条件下,同一种溶质在不同的溶剂中溶解度不同 |
下列叙述正确的是( )
| A、用稀硫酸除去NaCl溶液中少量的Na2CO3杂质 |
| B、将100 g溶质质量分数为98%的浓硫酸稀释为49%,需加水50 g |
| C、100 mL水和100 mL酒精混合后体积小于200 mL,说明分子间有间隔 |
| D、在不同的酸溶液中都含有相同的氢离子,所以,酸有一些相似的性质 |
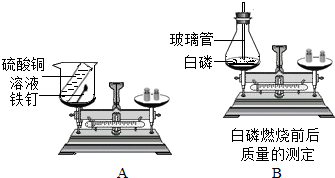
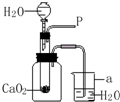 卫生部等7部委联合发布公告,禁止在面粉生产中添加过氧化钙(用作面粉增白).李明同学闻知后,对过氧化钙很感兴趣,就去买了一些回来做实验.
卫生部等7部委联合发布公告,禁止在面粉生产中添加过氧化钙(用作面粉增白).李明同学闻知后,对过氧化钙很感兴趣,就去买了一些回来做实验.