题目内容
19.下列括号中是除去少量杂质所用的方法或试剂,其中错误的是( )| A. | CaO中的CaCO3(高温煅烧) | B. | CO2中的CO(点燃) | ||
| C. | CO中的CO2(澄清的石灰水) | D. | N2中的O2(灼热铜丝) |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CaCO3固体高温煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、除去二氧化碳中的一氧化碳不能够点燃,这是因为当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;故选项所采取的方法错误.
C、CO2能与澄的清石灰水反应生成碳酸钙沉淀和水,CO不与澄清的清石灰水反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、氧气通过灼热的铜丝时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
10.掌握化学用语是学好化学的关键,下列化学用语与所表述的意义相符合的是( )
| A. | 2Ag--2个汞原子 | |
| B. | $\stackrel{+2}{Ca}$--每个钙离子带有2个单位的正电荷 | |
| C. | NO--1个一氧化氮分子 | |
| D. | 3Fe3+--3个亚铁离子 |
8.小强同学用三支试管,分别取适量的稀盐酸、澄清石灰水、碳酸钠溶液,进行相关实验探究.
步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,说明,Na2CO3溶液显碱性;步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含有A.
(选填答案:A.稀盐酸 B.澄清石灰水 C.碳酸钠溶液 )
【实验猜想】步骤3所得滤液中溶质可能为:
①NaCl Na2CO3; ②NaCl CaCl2和NaOH;③NaCl Na2CO3和NaOH④…..
【实验验证】(提示CaCl2溶液显中性)
【反思评价】有同学提出将CaCl2溶液改为稀盐酸,若观察到有气泡产生且红色消失,则证明猜想③成立.小刚同学认为不正确,其理由是:若改为稀盐酸,只能证明碳酸钠的存在,无法证明氢氧化钠的存在.
步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,说明,Na2CO3溶液显碱性;步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含有A.
(选填答案:A.稀盐酸 B.澄清石灰水 C.碳酸钠溶液 )
【实验猜想】步骤3所得滤液中溶质可能为:
①NaCl Na2CO3; ②NaCl CaCl2和NaOH;③NaCl Na2CO3和NaOH④…..
【实验验证】(提示CaCl2溶液显中性)
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入足量CaCl2溶液 | 有白色沉淀产生且红色不消失 | 猜想③成立 |
9.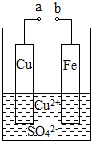 某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
 某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu | |
| C. | 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成棕黄色 | |
| D. | a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |